
【题目】已知:①A—I均为芳香族化合物,A的分子式为C8H10O, E的分子式为C7H7Cl,I的分子式为C23H22O3
②A的苯环上只有一个取代基,B能发生银镜反应,D的相对分子质量比C大4,E的核磁共振氢谱有3组峰
③![]()
④![]()
芳香酯I的合成路线如下:

请回答下列问题:
(1)A→B的反应类型为 ,E的名称为 ;
(2)E→F与F→G的顺序不能颠倒,理由是 ;
(3)B与银氨溶液反应的化学方程式为 ;
(4)I的结构简式为 ;
(5)符合下列要求A的同分异构体还有 种(不包括A);
①与Na反应并产生H2 ②芳香族化合物
(6)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
![]()
【答案】(1)氧化反应 对氯甲苯或4—氯甲苯
(2)如果颠倒则(酚)羟基会被KMnO4/H+氧化
(3)![]()
(4)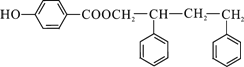 (5)13
(5)13
(6)![]()
【解析】
试题分析:A-I均为芳香族化合物,根据A的分子式可知A的侧链为饱和结构,A能够催化氧化生成B,B能够发生银镜反应,其能够发生信息反应③,则B分子中含有苯环和侧链-CH2CHO结构,故B的结构简式为![]() ,A为
,A为![]() ;B通过信息反应生成C,则C为
;B通过信息反应生成C,则C为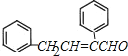 ,D比C的相对分子质量大4,恰好为2分子氢气,则说明C与氢气发生加成反应生成D,故D为
,D比C的相对分子质量大4,恰好为2分子氢气,则说明C与氢气发生加成反应生成D,故D为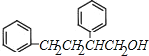 ;E的核磁共振氢谱有3组峰,E能够被酸性高锰酸钾溶液氧化,则E分子中含有甲基,且氯原子位于甲基的对位,故E为
;E的核磁共振氢谱有3组峰,E能够被酸性高锰酸钾溶液氧化,则E分子中含有甲基,且氯原子位于甲基的对位,故E为![]() ;E被酸性高锰酸钾溶液氧化成F,则F为
;E被酸性高锰酸钾溶液氧化成F,则F为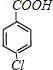 ;F在浓NaOH溶液中加热发生水解反应生成酚羟基和羧酸钠,然后在酸性条件下转化成G,则G为
;F在浓NaOH溶液中加热发生水解反应生成酚羟基和羧酸钠,然后在酸性条件下转化成G,则G为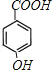 ;G和D发生酯化反应生成I,则I为
;G和D发生酯化反应生成I,则I为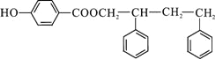 ;
;
(1)A→B为![]() 催化氧化生成
催化氧化生成![]() ,该反应为氧化反应;E为
,该反应为氧化反应;E为![]() ,氯原子位于4号C,其名称为4-氯甲苯或对氯甲苯;
,氯原子位于4号C,其名称为4-氯甲苯或对氯甲苯;
(2)E到G的反应中需要分别引进酚羟基和羧基,由于酚羟基容易被酸性高锰酸钾溶液氧化,所以E→F与F→G的顺序不能颠倒;
(3)B分子中含有醛基,能够与与银氨溶液发生反应生成单质银,反应的化学方程式为:![]() ;
;
(4)G和D发生酯化反应生成I,I的结构简式为: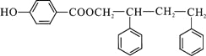 ;
;
(5)A为![]() ,①与Na反应并产生H2,说明该有机物分子中含有羟基;②芳香族化合物,有机物分子中含有苯环,满足条件的有机物分子中可能含有的侧链为:①-CH(OH)CH3,②-OH、-CH2CH3,③1个-CH3,1个-CH2OH,④1个-OH、2个-CH3,其中①存在1种结构,②③都存在邻、间、对3种结构,④:当3个取代基都在间位时存在1种结构,当3个取代基相邻时存在2种结构,当有2个取代基相邻时有3种结构,所以④总共有6种结构,根据以上分析可知,满足条件的有机物总共有:1+3+3+6=13种;
,①与Na反应并产生H2,说明该有机物分子中含有羟基;②芳香族化合物,有机物分子中含有苯环,满足条件的有机物分子中可能含有的侧链为:①-CH(OH)CH3,②-OH、-CH2CH3,③1个-CH3,1个-CH2OH,④1个-OH、2个-CH3,其中①存在1种结构,②③都存在邻、间、对3种结构,④:当3个取代基都在间位时存在1种结构,当3个取代基相邻时存在2种结构,当有2个取代基相邻时有3种结构,所以④总共有6种结构,根据以上分析可知,满足条件的有机物总共有:1+3+3+6=13种;
(6)CH3CH2OH为原料制备CH3CH2CH2CH2OH,先将乙醇催化氧化生成乙醛,然后让乙醛发生信息反应③生成CH3CH=CHCHO,与氢气加成生成CH3CH2CH2CH2OH,所以合成流程为:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.直径介于1nm~100nm之间的微粒称为胶体
B.电泳现象可证明胶体带电
C.渗析法可用于含有氯化钠的淀粉溶液的提纯
D.用含1molFeCl3的溶液可制得6.02×1023个Fe(OH)3胶体粒子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于药物的使用说法正确的是
A.因碘酒使蛋白质变性,故常用于外用消毒
B.使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验
C.长期大量使用阿司匹林可预防疾病,没有副作用
D.能用于治疗胃酸过多的抗酸药通常含有麻黄碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知:H2A的A2-可表示S2-、SO42-、SO32-、SiO32-或CO32-。
(1)常温下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液。有关微粒物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。请根据图示填空:
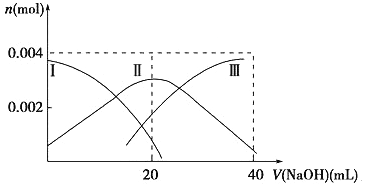
当V(NaOH)=20 mL时,溶液中离子浓度大小关系:____________。
②等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水____________(填“大”、“小”或“相等”)。
(2)若H2A为硫酸:t℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数KW=____________。
Ⅱ.已知:在25 ℃时 H2O![]() H++OH- KW=10-14
H++OH- KW=10-14
CH3COOH![]() H++CH3COO- Ka=1.8×10-5
H++CH3COO- Ka=1.8×10-5
(3)醋酸钠水解的平衡常数Kh具体数值=________________,
(4)0.5 mol·L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a,1 mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系为___________, a与b的关系为______________。(填“大于”“小于”或“等于”)
Ⅲ.(5)25 ℃时,将a mol·L-1的氨水与b mol·L-1盐酸等体积混合,反应后溶液恰好显中性,用a、b表示NH3·H2O的电离平衡常数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是( )
A. 向0.10mol·L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-)
B. 向0.10mol·L-1NaHSO3溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-)
C. 0.10mol·L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
D. 0.10mol·L-1CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等体积、等物质的量浓度的NH3HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.![]() <1.0×10-7mol·L-1
<1.0×10-7mol·L-1
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D.c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的化工产品,在工业上有重要的用途。某校化学兴趣小组,利用工业烧渣为原料,设计如下制备硫酸亚铁的方案。学生探究烧渣(主要成分为铁的氧化物及少量FeS、SiO2 等)制备绿矾(FeSO4·7H2O)。工艺流程如下所示:
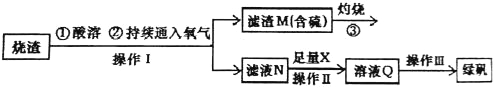
(1)烧渣在进行酸溶时用到了稀硫酸。他们在配制所需的稀硫酸时使用了自来水,有同学提出自来水中含有少量的Cl-,会影响到制出的FeSO4 的纯度。请你设计实验证明已配制的稀硫酸中混有Cl-。
_______________________。
(2)过程③灼烧时产生的气体通入下列溶液中,溶液不会褪色的是___________
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.红色的酚酞试液
(3)X 是 , 此时滤液N 中发生反应的离子方程式为 。检验溶液Q 中含有的金属阳离子的实验方法是 。
(4)操作III 的操作步骤为蒸发浓缩、 、过滤( 填操作名称)、 、干燥。
(5)硫酸亚铁可以用于治疗缺铁性贫血症,某严重贫血患者共需补充2.8g铁元素,服用的药品中相当于需要绿矾的质量为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com