
【题目】下列离子方程式书写正确的是( )
A.铜跟硝酸银溶液反应:Cu+Ag+=Cu2++Ag
B.硫酸与氢氧化钡溶液反应:H++![]() +Ba2++OH-=BaSO4↓+H2O
+Ba2++OH-=BaSO4↓+H2O
C.碳酸铵与盐酸反应:![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
D.Cu(OH)2与H2SO4溶液反应:H++OH-=H2O
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,满足图示转化关系的是( )

物质 选项 | 甲 | 乙 | 丙 | 戊 | 丁 |
A | Cu | HNO3 | Cu(NO3)2 | Fe | NO |
B | H2O | Fe | H2 | O2 | Fe2O3 |
C | Al | NaOH | H2 | Al2O3 | NaAlO2 |
D | CH3CHO | O2 | CH3COOH | H2 | H2O |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2mol水的摩尔质量和1mol水的摩尔质量
B.200mL1mol/L氯化钙溶液中c(Cl-)和100mL2mol/L氯化钾溶液中c(Cl-)
C.32g二氧化硫中氧原子数和标准状况下11.2L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,11.2LH2与11.2LD2所含的质子数均为NA
B.硅晶体中,有NA个Si原子就有4NA个Si—Si键
C.6.4g Cu与3.2g硫粉混合隔绝空气加热,充分反应后,转移电子书为0.2NA
D.用惰性电极电解食盐水,若导线中通过2NA个电子,则阳极产生22.4L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.H2SO3的电离方程式:H2SO32H++SO32
B.Na2CO3的水解方程式:CO32+2H2OH2CO3+2OH
C.NaHSO4在水溶液中的电离方程式:NaHSO4= Na++H++SO42
D.HS的水解方程式:HS+ H2OH3O++S2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A. WZ的水溶液呈碱性
B. 元素非金属性的顺序为X>Y>Z
C. Y的最高价氧化物的水化物是中强酸
D. 该新化合物中Y不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:

回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________。
(2)步骤②需要加热的目的是_________________,温度保持80~95 ℃,采用的合适加热方式是_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_________________(填标号)。

(3)步骤③中选用足量的H2O2,理由是_________________。分批加入H2O2,同时为了_________________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,结构简式如图所示,下列有关叙述中正确的是( )
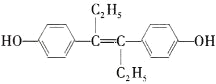
A.该有机物属于芳香烃
B.该有机物分子中,最多可能有18个碳原子共平面
C.该分子对称性好,所以没有顺反异构
D.该物质不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为25℃时,向25mL0.1mol·L-1NaOH溶液中逐滴滴加0.2mol·L-1CH3COOH溶液过程中混合溶液pH的变化曲线。
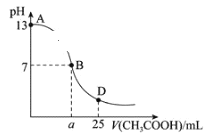
(1)NaOH与CH3COOH恰好完全反应时溶液中各离子浓度大小关系为__。
(2)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是__(填序号)。
A.c(OH-)一定大于c(CH3COO-) B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-) D.c(OH-)大于、小于或等于c(CH3COO-)
(3)在B点时,溶液中各离子浓度大小关系为__。
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)__2c(Na+)(填“>”“<”或“=”)。D点混合溶液的质子守恒的关系为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com