
【题目】0.25mol Na2SO4中所含的Na+离子个数约为 ( )
A.3.01×1023B.6.02×1023C.0.5 molD.1 mol
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是
A. 乙烯的结构筒式可以表示为CH2CH2 B. 苯、乙醇和乙酸都能发生取代反应
C. 乙醇和乙酸都存在碳氧双键 D. 液化石油气和天然气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为镁--次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是

A. 该燃料电池中镁为负极,发生还原反应
B. 电池的总反应式为Mg+ClO-+H2O===Mg(OH)2↓+Cl-
C. 放电过程中OH-移向负极
D. 酸性电解质的镁--过氧化氢燃料电池正极反应为:H2O2+2H++2e-===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布式为ns2np2 , 且原子半径是同族元素中最小的.
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有1个未成对电子.
③Z元素的电离能数据见表(kJ/mol):
I1 | I2 | I3 | I4 | … |
496 | 4562 | 6912 | 9540 | … |
请回答:
(1)Z2Y2的电子式为 , 含有的化学键类型 , Z2Y2为晶体.
(2)X、Y、Z三种元素所形成的常见化合物的名称为;XY2的结构式为 , 分子立体构型为 .
(3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是(填名称);晶体ZW的熔点比晶体XW4明显高的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为三种常见的单质,能发生如图1所示的转化关系,B的一种同素异形体的晶胞如图2所示。

回答下列问题:
(1)形成A的元素在周期表中的位置是__________________________________,A对应的基态原子的价电子排布为_____________________。
(2)在B单质对应的基态原子中,核外存在___________对自旋方向相反的电子。
(3)写出Y的一种常见等电子体分子的结构式__________________________;两者相比较沸点较高的是__________(填化学式);Y分子中B对应原子的杂化方式为_________________。
(4)配合物A(Y)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断A(Y)x晶体属于________________(填晶体类型)。A(Y)x的中心原子价电子数与配体提供的电子数之和为18,则x=__________。A(Y)x在一定条件下发生反应A(Y)x (s) ![]() A (s) + x Y (g),已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型是_____________。
A (s) + x Y (g),已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型是_____________。
(5)在图2晶胞中,每个晶胞平均占有__________个原子,若距离最近的两个原子的距离为L cm,晶胞边长为a cm,根据硬球接触模型,则L=_________a,晶胞的密度ρ=___________g·cm-3(用含a、NA代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度,相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分別为( )![]()
A.NH4Cl、(NH4)2SO4、CH3COONa
B.(NH4)2SO4、NH4Cl、CH3COONa
C.(NH4)2SO4、NH4Cl、NaOH
D.CH3COONa、NH4Cl、(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从植物花朵中提取到一种色素,它实际上是一种有机弱酸,可用HR表示,HR在盐酸溶液中呈现红色,HR在NaOH溶液中呈现蓝色,将HR加入浓硝酸中呈现红色,微热后溶液的红色褪去,根据以上现象,可推测( )
A.HR应为红色 B.HR应为蓝色
C.R-应为无色 D.R- 应为红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质N2、H2O、Na2O2、CaCl2、KOH、NaF中,既含有离子键,又含有共价键的物质是_______,属于共价化合物的是__________。
(2)用电子式表示CaCl2的形成过程: __________。
(3)氮化钠(Na3N)是科学家制备的种重要化合物,它与水作用产生NH3。请写出Na3N的电子式是__________。
(4)Na3N与盐酸反应生成两种盐,反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
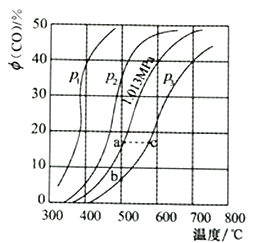
【题目】现将定量的H2O与足量碳在体积可变的恒压密闭容器中发生反应:
C(s)+H2O (g) ![]() CO(g)+H2(g)△H,测得压强、温度对CO的平衡组成的影响如图所示。
CO(g)+H2(g)△H,测得压强、温度对CO的平衡组成的影响如图所示。
(1)已知:2H2 (g)+O2(g)==2H2O (g) △H1
2CO(g)+ O2 (g)==2CO2(g)△H2
C(s)+ O2 (g)==CO2(g) △H3
则△H=_________(用含△H1、△H2、△H3的式子表示)。
(2)①下列措施能够提高H2产率的是_______(填标号)
a.加压 b.分离出CO C.加热 d.增大碳固体的量
②a、b、c三点所对应的水的转化率最小的是______________。
(3)700℃、P3时,将1molH2O与足量碳充入初始体积为1L的密闭容器中,恒温、恒压条件下,当反应进行到10min时,测得容器中H2的物质的量为0.12mol。
①10min内CO的平均反应速率为__________________ mol·L-1·min-1(保留两位有效数字)。
②此温度下该反应的平衡常数K___________。
③向容器中投料后,在下图中画出从0时刻到t1时刻达到平衡时容器中混合气体的平均摩尔质量的变化曲线。___________________
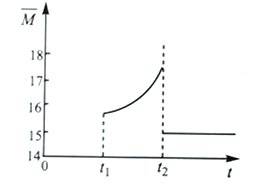
④从t1时刻开始,保持温度不变,对容器加压,混合气体平均摩尔质量从t2时刻后变化如上图,出现该变化的原因是____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com