
| 温度/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| K1 |
| K2 |
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| K1 |
| K2 |
| 1.47 |
| 2.38 |


科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中滴加盐酸酸化的氯化钡溶液 | 出现白色沉淀 | 该溶液中一定存在SO42 |
| B | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | -两者均能与盐酸反应 |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 上层溶液 显紫红色 | 氧化性:Fe3+>I2 |
| A、A | B、B | C、C | D、D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | X | Y | Z | W | 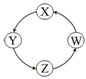 |
| ① | Cu | CuSO4 | Cu(OH)2 | CuO | |
| ② | Na | NaOH | Na2CO3 | NaCl | |
| ③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
| ④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
| A、①②③ | B、①③④ |
| C、②③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B、NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C、Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| D、NaHCO3溶液:c(Na+)+c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-o |
| 键能(Kj/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体的颜色变浅 |
| B、混合气体的物质的量相等 |
| C、混合气中NO2、NO、O2物质的量之比为2:2:1 |
| D、单位时间内生成2nmolNO同时生成2nmolNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑ |
| B、稀硫酸与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓ |
| C、盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、把金属钠放入水中:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com