
”¾ĢāÄæ”æijŠĖȤŠ”×éŅŌ·ĻĢśŠ¼ÖʵĆĮņĖįŃĒĢśļ§ŗ󣬰“ĻĀĮŠĮ÷³ĢÖʱø¶žĖ®ŗĻ²ŻĖįŃĒĢś(FeC2O4”¤2H2O)£¬½ųŅ»²½Öʱøøß“æ¶Č»¹ŌĢś·Ū”£

ŅŃÖŖ£ŗFeC2O4”¤2H2OÄŃČÜÓŚĖ®£¬150”ęæŖŹ¼Ź§½į¾§Ė®£»H2C2O4Ņ×ČÜÓŚĖ®£¬Čܽā¶ČĖęĪĀ¶ČÉżø߶ųŌö“ó”£
Ēė»Ų“š£ŗ
£Ø1£©ĻĀĮŠ²Ł×÷»ņĆčŹöÕżČ·µÄŹĒ__________”£
A.²½Öč¢Ś£¬H2C2O4ÉŌ¹żĮæÖ÷ŅŖŹĒĪŖĮĖŅÖÖĘFe2+Ė®½ā
B.²½Öč¢Ū£¬²ÉÓĆČČĖ®Ļ“µÓæÉĢįøß³żŌÓŠ§¹ū
C.²½Öč¢Ū£¬ÄøŅŗÖŠµÄČÜÖŹÖ÷ŅŖŹĒ(NH4)2SO4 ŗĶH2C2O4
D.²½Öč¢Ū£¬Čē¹ūŌŚ³£Ń¹ĻĀæģĖŁøÉŌļ£¬ĪĀ¶ČæÉŃ”ŌńĀŌøßÓŚ100”ę
£Ø2£©ČēĶ¼×°ÖĆ£¬¾¹żŅ»ĻµĮŠ²Ł×÷Ķź³É²½Öč¢ŪÖŠµÄ³éĀĖŗĶĻ“µÓ”£ĒėŃ”ŌńŗĻŹŹµÄ±ąŗÅ£¬°“ÕżČ·µÄ²Ł×÷Ė³Šņ²¹³äĶźÕū(Ļ“µÓ²Ł×÷Ö»Ščæ¼ĀĒŅ»“Ī)£ŗ
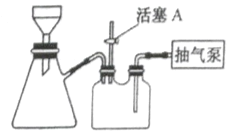
æŖ³éĘų±Ć”śa”śb”śd”ś_________”śc”ś¹Ų³éĘų±Ć
a.×ŖŅĘ¹ĢŅŗ»ģŗĻĪļ£» b.¹Ų»īČūA£» c.æŖ»īČūA£» d.Č·ČĻ³éøÉ£» e.¼ÓĻ“µÓ¼ĮĻ“µÓ”£
£Ø3£©³ĘČ”Ņ»¶ØĮæµÄFeC2O4”¤2H2OŹŌŃł£¬ÓĆĮņĖįČܽā£¬²ÉÓĆKMnO4µĪ¶Ø·Ø²ā¶Ø£¬ÕŪĖć½į¹ūČēĻĀ£ŗ
n (Fe2+)/mol | n (C2O42£)/mol | ŹŌŃłÖŠFeC2O4”¤2H2OµÄÖŹĮæ·ÖŹż |
9.80”Į10£4 | 9.80”Į10£4 | 0.980 |
ÓɱķÖŠŹż¾ŻĶĘ²āŹŌŃłÖŠ×īÖ÷ŅŖµÄŌÓÖŹŹĒ___________
£Ø4£©ŹµĻÖ²½Öč¢Ü±ŲŠėÓƵ½µÄĮ½ÖÖŅĒĘ÷ŹĒ_________(¹©Ń”ŅĒĘ÷£ŗa.ÉÕ±£»b.ŪįŪö£»c.ÕōĮóÉÕĘ棻d.øßĪĀĀÆ£»e.±ķĆęĆó£»f.׶ŠĪĘæ)£»øĆ²½ÖčµÄ»Æѧ·½³ĢŹ½ŹĒ______________________”£
£Ø5£©ĪŖŹµĻÖ²½Öč¢Ż£¬²»ŅĖÓĆĢ¼·Ū»¹ŌFe2O3£¬ĄķÓÉŹĒ________________”£
”¾“š°ø”æBD c”śe”śb”śd (NH4)2SO4 bd 4FeC2O4”¤2H2O+3O2![]() 2Fe2O3+8CO2+8H2O ÓĆĢæ·Ū»¹Ō»į½ųŌÓÖŹ
2Fe2O3+8CO2+8H2O ÓĆĢæ·Ū»¹Ō»į½ųŌÓÖŹ
”¾½āĪö”æ
ĮņĖįŃĒĢśļ§¾§ĢåČܽāÓŚĖ®£¬ĪŖ±£Ö¤Fe2+ĶźČ«·“Ó¦£¬Ķ¬Ź±·ĄÖ¹Fe2+±»Ńõ»Æ£¬ŠčŅŖ¼ÓČė¹żĮæµÄ²ŻĖį£¬Éś³ÉµÄ²ŻĖįŃĒĢś¾§Ģå£ØFeC2O4”¤2H2O£©ÄŃČÜÓŚĖ®£¬æÉĶعż³éĀĖ”¢Ļ“µÓ²¢øÉŌļ»ńµĆ£¬½«ĖłµĆ¾§ĢåŌŚæÕĘųÖŠ×ĘÉÕ£¬µĆ“æŃõ»ÆĢś£ØFe2O3£©£¬ŌŁÓĆCO»¹ŌŃõ»ÆĢśµĆµ½»¹ŌĢś·Ū£¬¾Ż“Ė½ā“š”£
ĮņĖįŃĒĢśļ§¾§ĢåČܽāÓŚĖ®£¬ĪŖ±£Ö¤Fe2+ĶźČ«·“Ó¦£¬Ķ¬Ź±·ĄÖ¹Fe2+±»Ńõ»Æ£¬ŠčŅŖ¼ÓČė¹żĮæµÄ²ŻĖį£¬Éś³ÉµÄ²ŻĖįŃĒĢś¾§Ģå£ØFeC2O4”¤2H2O£©ÄŃČÜÓŚĖ®£¬æÉĶعż³éĀĖ”¢Ļ“µÓ²¢øÉŌļ»ńµĆ£¬½«ĖłµĆ¾§ĢåŌŚæÕĘųÖŠ×ĘÉÕ£¬µĆ“æŃõ»ÆĢś£ØFe2O3£©£¬ŌŁÓĆCO»¹ŌŃõ»ÆĢśµĆµ½»¹ŌĢś·Ū£»
£Ø1£©AĻī£¬²½Öč¢ŁČܽāĖį»ÆŗóČÜŅŗŅŃ³ŹĖįŠŌ£¬¹Ź²½Öč¢ŚŹ±H2C2O4ÉŌ¹żĮæµÄÖ÷ŅŖÄæµÄ²»ŹĒĖį»ÆŅÖÖĘFe2+Ė®½ā£¬¶ųŹĒ±£Ö¤Fe2+ĶźČ«×Ŗ»ÆĪŖ²ŻĖįŃĒĢś¾§Ģ壬Ķ¬Ź±·ĄÖ¹Fe2+±»Ńõ»Æ£¬ĢįøßŌĮĻĄūÓĆĀŹ£¬¹ŹAĻī“ķĪó£»
BĻī£¬²½Öč¢Ū£¬²ÉÓĆČČĖ®Ļ“µÓæÉĢįøß²ŻĖįµÄČܽā¶Č£¬ĢįÉż³żŌÓŠ§¹ū£¬¹ŹBĻīÕżČ·£»
CĻī£¬Ėį»ÆŗĶ¼ÓČėÉŌ¹żĮæµÄH2C2O4ŗ󣬷¢Éś·“Ó¦(NH4)2Fe(SO4)2+ H2C2O4+2H2O= FeC2O4”¤2H2O”ż+(NH4)2SO4+H2SO4,¹ŹÄøŅŗÖŠµÄČÜÖŹÖ÷ŅŖÓŠ(NH4)2SO4”¢H2SO4ŗĶH2C2O4,¹ŹCĻī“ķĪó£»
DĻī£¬øł¾ŻĢāøųŠÅĻ¢£¬FeC2O4”¤2H2O ŌŚ150”ęæŖŹ¼Ź§½į¾§Ė®£¬¹ŹĀŌøßÓŚ100”ę²»Ó°Ļģ²śĪļµÄ³É·Ö£¬ĪŖŹ¹FeC2O4”¤2H2OæģĖŁøÉŌļ£¬æÉŹ¹ĪĀ¶ČøßÓŚ100”ę£¬µ«ŠėµĶÓŚ150”ę£¬¹ŹDĻīÕżČ·£»
×ŪÉĻĖłŹö£¬±¾ĢāÕżČ·“š°øĪŖBD”£
£Ø2£©³éĀĖĶź³Éŗ󣬊čŅŖĻ“µÓ¾§Ģ壬¹ŹÓ¦øĆĻČ“ņæŖ»īČūA£¬Ź¹ĪüĀĖĘæÄŚµÄŃ¹Ēæ»ŲÉż£¬Č»ŗóĢķ¼ÓĻ“µÓ¼Į£¬“żĻ“µÓ¼Į»ŗĀżĶعż¾§Ģåŗó¹Ų±Õ»īČūA£¬ŌŁ“ĪČ·ČĻ³éøÉ£¬“ņæŖ»īČūA·ĄÖ¹·¢Éśµ¹Īü£¬×īŗó¹Ų±ÕĘų±Ć£¬ÕżČ·µÄĖ³ŠņĪŖæŖ³éĘų±Ć”ś×ŖŅĘ¹ĢŅŗ»ģŗĻĪļ”ś¹Ų»īČūA”śČ·ČĻ³éøÉ”ś¹Ų»īČūA”śČ·ČĻ³éøÉ”śæŖ»īČūA”ś¹Ų³éĘų±Ć£¬
¹Ź“š°øĪŖ£ŗc”śe”śb”śd£»
£Ø3£©ÓÉĶ¼±ķŹż¾ŻæÉÖŖ£¬ČÜŅŗÖŠŅŃÖŖFe2+ŗĶC2O42-µÄÅضČĀś×ćµēŗÉŹŲŗć£¬ĖµĆ÷ŌÓÖŹÖŠ²»“ęŌŚFe2+»ņC2O42-£¬ÄĒŌÓÖŹÖ»ÄÜŹĒ·“Ó¦µÄĮķŅ»ÖÖÉś³ÉĪļ(NH4)2SO4”£
¹Ź“š°øĪŖ£ŗ(NH4)2SO4£»
£Ø4£©¹ĢĢå×ĘÉÕŠčŅŖŌŚŪįŪöÄŚ½ųŠŠ£¬ŌņĖłŠčŅŖµÄŅĒĘ÷ÓŠŪįŪö¼°¼ÓČČĖłŠčµÄøßĪĀĀÆ£¬ÓƵ½µÄĮ½ÖÖŅĒĘ÷ŹĒbd£»²ŻĖįŃĒĢśŗĶO2×ĘÉÕŹ±·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ4FeC2O4”¤2H2O+3O2![]() 2Fe2O3+8CO2+8H2O ”£
2Fe2O3+8CO2+8H2O ӣ
¹Ź“š°øĪŖ£ŗbd£»4FeC2O4”¤2H2O+3O2![]() 2Fe2O3+8CO2+8H2O £»
2Fe2O3+8CO2+8H2O £»
£Ø5£©²½Öč¢ŻŃ”ÓĆĢ¼·Ū»¹ŌFe2O3£¬¶ąÓąµÄĢ¼·Ū»įÓ°ĻģĢś·ŪµÄ“æ¶Č”£
¹Ź“š°øĪŖ£ŗÓĆĢæ·Ū»¹Ō»įŅż½ųŌÓÖŹ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ2X(g)+Y(g)![]() 2Z(g)£¬·“Ó¦ÖŠ¦Ų£ØZµÄĪļÖŹµÄĮæ·ÖŹż£©ĖęĪĀ¶ČTµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
2Z(g)£¬·“Ó¦ÖŠ¦Ų£ØZµÄĪļÖŹµÄĮæ·ÖŹż£©ĖęĪĀ¶ČTµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
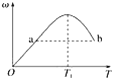
A. T1Ź±£¬vÕż£¾vÄę
B. Õż·“Ó¦µÄ¦¤H£¼0
C. a”¢bĮ½µćµÄ·“Ó¦ĖŁĀŹv(a)=v(b)
D. µ±ĪĀ¶ČµĶÓŚT1Ź±£¬¦ŲŌö“óµÄŌŅņŹĒĘ½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”«I·Ö±š±ķŹ¾ÖŠŃ§»Æѧ֊³£¼ūµÄŅ»ÖÖĪļÖŹ£¬ĘäÖŠA”¢IĪŖ³£¼ū½šŹō£¬ĖüĆĒÖ®¼äµÄĻą»„¹ŲĻµČēĶ¼ĖłŹ¾(²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļƻӊĮŠ³ö)£¬ĒŅŅŃÖŖGĪŖÖ÷×åŌŖĖŲµÄ¹ĢĢ¬Ńõ»ÆĪļ£¬A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹÖŠ¾łŗ¬Ķ¬Ņ»ÖÖŌŖĖŲ”£ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ

£Ø1£©A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹÖŠĖłŗ¬Ķ¬Ņ»ÖÖŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ________”£
£Ø2£©Š“³öCĪļÖŹµÄ»ÆѧŹ½£ŗ________”£
£Ø3£©Š“³ö¢Ł”¢¢Ž·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
¢Ł£ŗ____________________________”£
¢Ž£ŗ____________________________”£
£Ø4£©“ÓÄÜĮæ±ä»ÆµÄ½Ē¶Čæ“£¬·“Ó¦¢Ł¢Ś¢ŪÖŠ£¬ŹōÓŚ·ÅČČ·“Ó¦µÄŹĒ________(ĢīŠņŗÅ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§ÓĆŗ¬½į¾§Ė®µÄÕżŃĪX(ĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ×é³ÉµÄ“æ¾»Īļ)½ųŠŠĮĖČēĻĀŹµŃé£ŗ
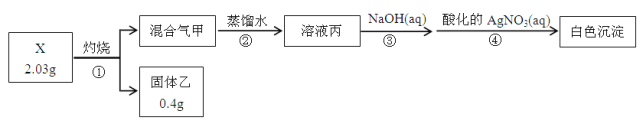
ŹµŃéÖŠ¹Ū²āµ½£ŗ»ģŗĻĘų¼×³ŹĪŽÉ«²¢±»ÕōĮóĖ®Č«²æĪüŹÕ£»¹ĢĢåŅŅĪŖ“æ¾»Īļ£»ŌŚ²½Öč¢ŪÖŠ£¬Č”1/10ČÜŅŗ±ū£¬Ē”ŗĆÖŠŗĶŠčĻūŗÄ0.00200molNaOH£»ĮķČ”Ņ»¶ØĮæµÄČÜŅŗ±ū£¬¼ÓČėÉŁĮæK2FeO4¹ĢĢ壬²śÉś»ĘĀĢÉ«ĘųĢ唣
Ēė»Ų“š£ŗ
£Ø1£©XµÄ»ÆѧŹ½ŹĒ__________£¬²½Öč¢ŁµÄ»Æѧ·½³ĢŹ½ŹĒ______________________________”£
£Ø2£©ČÜŅŗ±ūÓėK2FeO4¹ĢĢå·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_____________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹæÉÓĆ×÷Ź³Ę·Ģķ¼Ó¼ĮµÄŹĒ£Ø £©
A.CH3OHB.SO2C.HCHOD.I2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃŠ¾æŠ”×é°“ĻĀĮŠĀ·ĻßŗĻ³Éæ¹ŅÖÓōŅ©ĪļĀšĀȱ“°·
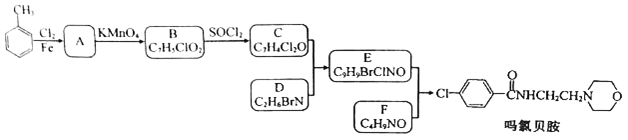
ŅŃÖŖ£ŗ
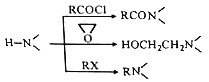
Ēė»Ų“š£ŗ
£Ø1£©ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ________”£
A. »ÆŗĻĪļAÄÜ·¢Éś»¹Ō·“Ó¦ B. »ÆŗĻĪļBÄÜÓėĢ¼ĖįĒāÄĘ·“Ó¦²śÉśĘųĢå
C. »ÆŗĻĪļD¾ßÓŠ¼īŠŌ D. ĀšĀȱ“°·µÄ»ÆѧŹ½ŹĒC13H13ClN2O2
£Ø2£©»ÆŗĻĪļFµÄ½į¹¹¼ņŹ½ŹĒ_____________”£
£Ø3£©Š“³öC+D”śEµÄ»Æѧ·½³ĢŹ½______________________”£
£Ø4£©ĪŖĢ½Ė÷ŠĀµÄŗĻ³ÉĀ·Ļߣ¬·¢ĻÖÓĆ»ÆŗĻĪļCÓėX(C6H14N2O)Ņ»²½·“Ó¦¼“æÉŗĻ³ÉĀšĀȱ“°·”£ĒėÉč¼ĘŅŌ»·ŃõŅŅĶé(![]() )ĪŖŌĮĻŗĻ³ÉXµÄŗĻ³ÉĀ·Ļß___________(ÓĆĮ÷³ĢĶ¼±ķŹ¾£¬ĪŽ»śŹŌ¼ĮČĪŃ”)”£
)ĪŖŌĮĻŗĻ³ÉXµÄŗĻ³ÉĀ·Ļß___________(ÓĆĮ÷³ĢĶ¼±ķŹ¾£¬ĪŽ»śŹŌ¼ĮČĪŃ”)”£
£Ø5£©Š“³ö»ÆŗĻĪļX(C6H14N2O)æÉÄܵÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½_____________”£ŠėĶ¬Ź±·ūŗĻ£ŗ¢Ł·Ö×ÓÖŠÓŠŅ»øöĮłŌŖ»·£¬ĒŅ³É»·Ō×ÓÖŠ×ī¶ąŗ¬Ņ»øö·ĒĢ¼Ō×Ó”£¢Ś1H£NMRĘ×ĻŌŹ¾·Ö×ÓÖŠÓŠ5ÖÖĒāŌ×Ó£»IRĘ×±ķĆ÷·Ö×ÓÖŠÓŠN£N¼ü£¬ĪŽ O£H¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢś“„Ć½ŹĒÖŲŅŖµÄ“߻ƼĮ£¬COŅ×ÓėĢś“„Ć½×÷ÓƵ¼ÖĀĘ䏧Ȅ“߻ƻīŠŌ£ŗFe+5CO=Fe(CO)5£»³żČ„COµÄ»Æѧ·“Ó¦ĪŖ£ŗ[Cu(NH3)2]OOCCH3+CO+NH3£½[Cu(NH3)3(CO)]OOCCH3”£
(1)»łĢ¬FeŌ×ÓµÄĶāĪ§µē×ÓÅŲ¼Ź½£ŗ________£¬C”¢N”¢OµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņĪŖ________”£
£Ø2£©Fe(CO)5ÓÖĆūōŹ»łĢś£¬³£ĪĀĻĀĪŖ»ĘÉ«ÓĶדŅŗĢ壬ŌņFe(CO)5µÄ¾§ĢåĄąŠĶŹĒ_______£¬ÓėCO»„ĪŖµČµē×ÓĢåµÄ·Ö×ӵĵē×ÓŹ½ĪŖ______________”£
£Ø3£©ĻõĖį¼ŲÖŠNO3-µÄæռ乹ŠĶ_______£¬·Ö×ÓÖŠµÄ“󦊼üæÉÓĆ·ūŗÅ![]() ±ķŹ¾£¬ĘäÖŠm“ś±ķ²ĪÓėŠĪ³ÉµÄ“󦊼üŌ×ÓŹż£¬n“ś±ķ²ĪÓėŠĪ³ÉµÄ“󦊼üµē×ÓŹż£ØČē±½·Ö×ÓÖŠµÄ“󦊼üæɱķŹ¾ĪŖ
±ķŹ¾£¬ĘäÖŠm“ś±ķ²ĪÓėŠĪ³ÉµÄ“󦊼üŌ×ÓŹż£¬n“ś±ķ²ĪÓėŠĪ³ÉµÄ“󦊼üµē×ÓŹż£ØČē±½·Ö×ÓÖŠµÄ“󦊼üæɱķŹ¾ĪŖ![]() £©£¬ŌņNO3-ÖŠµÄ“󦊼üÓ¦±ķŹ¾ĪŖ____________”£
£©£¬ŌņNO3-ÖŠµÄ“󦊼üÓ¦±ķŹ¾ĪŖ____________”£
£Ø4£©ÅäŗĻĪļ[Cu(NH3)2]OOCCH3ÖŠĢ¼Ō×ÓµÄŌÓ»ÆĄąŠĶŹĒ________£¬ÅäĪ»ĢåÖŠĢį¹©¹Ā¶Ōµē×ÓµÄŌ×ÓŹĒ_____”£
£Ø5£©ÓĆ[Cu(NH3)2]OOCCH3³żČ„COµÄ·“Ó¦ÖŠ£¬æĻ¶ØÓŠ______ŠĪ³É£®
a£®Ąė×Ó¼ü b£®ÅäĪ»¼ü c£®·Ē¼«ŠŌ¼ü d£®¦Ņ¼ü
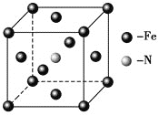
£Ø6£©ĢśŗĶ°±ĘųŌŚ640 ”ęæÉ·¢ÉśÖĆ»»·“Ó¦£¬²śĪļÖ®Ņ»µÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½__________________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗ£¬ĻĀĮŠ²Ł×÷»įŌģ³É½į¹ūĘ«øߵďĒ£Ø £©
A.³ĘĮæ¹ĢĢåNaOHŹ±£¬ÓŠ³±½āĻÖĻóB.ČܽāŗóŅĘŅŗÖĮČŻĮæĘæÖŠ£¬Ī“ĄäČ“ČÜŅŗ
C.Ī“½«Ļ“µÓÉÕ±µÄĖ®×ŖŅĘÖĮČŻĮæĘæÖŠD.¶ØČŻŹ±ŃöŹÓ¶ĮŹż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃŠ¾æČĖŌ±“Óľ¶ś²ĖÖŠĢįČ”¹żŃõ»ÆĪļĆø£ØPOD£©£¬·Ö±šÓėĖÄÖÖ²»Ķ¬·ÓĄąĪļÖŹ¼°H2O2½ųŠŠ“߻Ʒ“Ó¦£¬½į¹ūČēĶ¼ĖłŹ¾”£ĻĀĮŠĻą¹ŲĖµ·ØÕżČ·µÄŹĒ
””””””””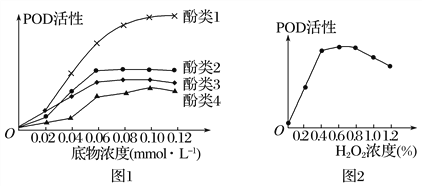
A. Ķ¼1ĖłŹ¾µÄŹµŃéÄæµÄŹĒĢ½¾æ²»Ķ¬·ÓĄąĪļÖŹµÄÅØ¶Č¶ŌPOD»īŠŌµÄÓ°Ļģ
B. µ±µ×ĪļÅضČĪŖ0.08 mmolL£1Ź±£¬POD“ß»Æ·ÓĄą2µÄ·“Ó¦ĖŁĀŹŅ»¶Ø“óÓŚ·ÓĄą3
C. ÓÉĶ¼2æÉÖŖ£¬H2O2ÅØ¶Č¹żøß»įŅÖÖĘPODµÄ»īŠŌ£¬½µµĶÅضČŗóPODµÄ»īŠŌŅ»¶Ø»į»Öø“
D. H2O2¶ŌPOD»īŠŌµÄÓ°ĻģÓėĪĀ¶ČŗĶpH¶ŌPOD»īŠŌµÄÓ°ĻģĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com