


科目:高中化学 来源: 题型:
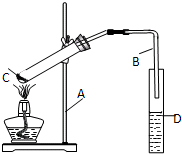 实验室制乙酸乙脂的装置如图:
实验室制乙酸乙脂的装置如图:查看答案和解析>>
科目:高中化学 来源: 题型:
 所示:
所示:查看答案和解析>>
科目:高中化学 来源: 题型:
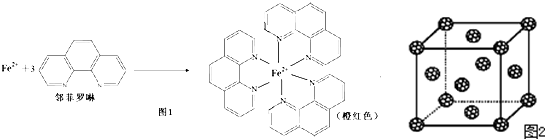
查看答案和解析>>
科目:高中化学 来源: 题型:
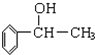
 ,这种醇的结构简式可能为( )
,这种醇的结构简式可能为( )| A、CH2=CHCH2OH |
| B、CH2ClCHClCH2OH |
| C、CH3CH2OH |
| D、CH3CH(OH)CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na | B、Cl | C、Br | D、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用电解熔融氯化钠的方法得到活泼金属钠 |
| B、在加热的情况下利用氢气还原三氧化二铝得到金属铝 |
| C、用铝热反应原理炼得熔点较高的金属铬 |
| D、热分解法直接加热HgO得到金属Hg |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com