
科目:高中化学 来源: 题型:
 (2010?卢湾区二模)氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3--SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
(2010?卢湾区二模)氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3--SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.如图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
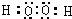
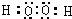
| ||
| ||
| 2×24a |
| 22.4×5 |
| 3a |
| 7 |
| 2×24a |
| 22.4×5 |
| 3a |
| 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
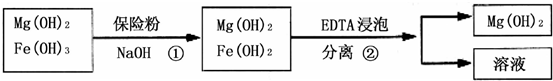
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
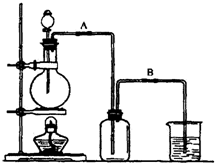 某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:
某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com