
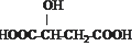
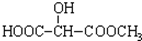 B£®
B£®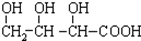 C£®H3COOC-COOCH3
C£®H3COOC-COOCH3 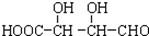 E£®
E£®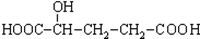
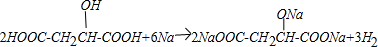 £®
£® ·ÖĪö £Ø1£©øĆÓŠ»śĪļÖŠŗ¬ÓŠōĒ»łŗĶōČ»ł£¬ĖłŅŌ¾ßÓŠōČĖįŗĶ“¼µÄŠŌÖŹ£»
£Ø2£©·Ö×ÓŹ½ĻąĶ¬½į¹¹²»Ķ¬µÄ»ÆŗĻĪļ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬°üĄØĢ¼Į“Ņģ¹¹”¢¹ŁÄÜĶÅŅģ¹¹£»
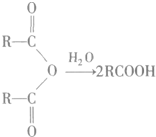
£Ø3£©ōČ»łŗĶōĒ»ł¶¼ÄÜŗĶÄĘ·“Ӧɜ³ÉĒāĘų£®
½ā“š ½ā£ŗ£Ø1£©øĆÓŠ»śĪļÖŠŗ¬ÓŠōĒ»łŗĶōČ»ł£¬ĖłŅŌ¾ßÓŠōČĖįŗĶ“¼µÄŠŌÖŹ£¬ÄÜŗĶōČĖį»ņ“¼·¢ÉśČ”“ś·“Ó¦£¬ÄÜŗĶĒāŃõ»ÆÄĘ·¢ÉśÖŠŗĶ·“Ó¦£¬Į¬½Ó“¼ōĒ»łĻąĮŚµÄĢ¼Ō×ÓÉĻŗ¬ÓŠĒāŌ×Ó£¬ĖłŅŌÄÜ·¢ÉśĻūČ„·“Ó¦£¬¹ŹŃ”BDF£¬
¹Ź“š°øĪŖ£ŗōČ»ł”¢ōĒ»ł£»BDF£»
£Ø2£©·Ö×ÓŹ½ĻąĶ¬½į¹¹²»Ķ¬µÄ»ÆŗĻĪļ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬°üĄØĢ¼Į“Ņģ¹¹”¢¹ŁÄÜĶÅŅģ¹¹£®
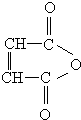
AŗĶDÓėXµÄ·Ö×ÓŹ½ĻąĶ¬£¬½į¹¹²»Ķ¬£¬ĖłŅŌŹĒĶ¬·ÖŅģ¹¹Ģ壻BŗĶXŗ¬ÓŠµÄĒāŌ×ÓøöŹż²»Ķ¬£¬CŗĶXŗ¬ÓŠµÄŃõŌ×ÓøöŹż²»Ķ¬£¬EŗĶXŗ¬ÓŠµÄĢ¼Ō×ÓøöŹż²»Ķ¬£¬ĖłŅŌB”¢C”¢EŗĶX²»ŹĒĶ¬·ÖŅģ¹¹Ģ壬¹Ź“š°øĪŖ£ŗAD£»
£Ø3£©ōČ»łŗĶōĒ»ł¶¼ÄÜŗĶÄĘ·“Ӧɜ³ÉĒāĘų£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ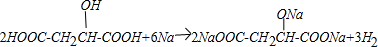 ”ü£¬
”ü£¬
¹Ź“š°øĪŖ£ŗ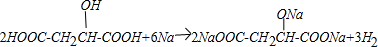 ”ü£®
”ü£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ»śĪļµÄŠŌÖŹ”¢Ķ¬·ÖŅģ¹¹ĢåµÄÅŠ¶ĻµČÖŖŹ¶µć£¬ÄŃ¶Č²»“ó£¬ĻČÅŠ¶ĻÓŠ»śĪļŗ¬ÓŠµÄ¹ŁÄÜĶÅŌŁČ·¶ØĘäŗ¬ÓŠµÄŠŌÖŹ£¬½į¹¹¾ö¶ØŠŌÖŹ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¢ŚRCOOH$\stackrel{LiAlH_{4}}{”ś}$RCH2OH
¢ŚRCOOH$\stackrel{LiAlH_{4}}{”ś}$RCH2OH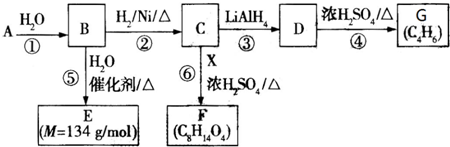
 £®
£® £®
£®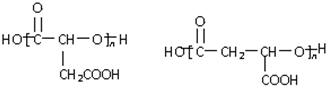 £®
£®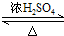 CH3CH2OOCCH2CH2COOCH2CH3+2H2O£®
CH3CH2OOCCH2CH2COOCH2CH3+2H2O£®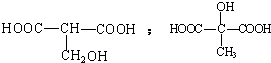 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SŗĶSO2 | B£® | O2ŗĶSO2 | C£® | H2S»ņSO2 | D£® | Ö»ÓŠSO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ū¢Ü | C£® | ¢Ł¢Ū | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 Ӣ
”¢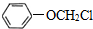 £ØŠ“Į½ÖÖ£©
£ØŠ“Į½ÖÖ£©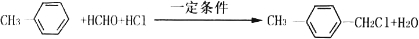 £¬
£¬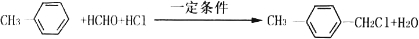 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōö¼Ó6.5g | B£® | ¼õÉŁ6.5g | C£® | ¼õÉŁ5.6g | D£® | Ōö¼Ó6.4g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4NO3 | B£® | £ØNH4£©2CO3 | C£® | NH4CNO | D£® | CH3COONH4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
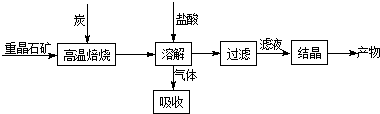
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com