
【题目】有效脱除烟气中的SO2是环境保护的重要课题。
(1)氨水可以脱除烟气中的SO2。氨水脱硫的相关热化学方程式如下:
2NH3(g) +H2O(l) +SO2(g) =(NH4)2SO3(aq) ΔH= akJ·mol1
(NH4)2SO3(aq)+H2O(l) +SO2(g) =2NH4HSO3(aq) ΔH = bkJ·mol1
2(NH4)2SO3(aq) +O2(g) =2(NH4)2SO4(aq) ΔH =ckJ·mol1
反应NH3(g) +NH4HSO3(aq) +![]() O2(g) = (NH4)2SO4(aq)的ΔH=____kJ·mol1。
O2(g) = (NH4)2SO4(aq)的ΔH=____kJ·mol1。
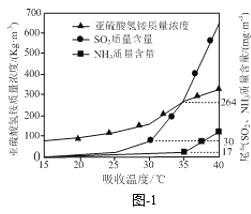
已知:SO2的国家排放标准为80mg·m3。氨水脱除烟气中的SO2是在吸收塔中进行的,控制其他实验条件相同,仅改变吸收塔的温度,实验结果如题图-1所示,为了尽可能获得NH4HSO3,则吸收塔合适的温度约为________。
A.25℃ B.31℃ C.35℃
(2)电解法可以脱除烟气中的SO2。用Na2SO4溶液吸收烟气中的SO2,使用惰性电极电解吸收后的溶液,H2SO3在阴极被还原为硫单质,阴极的电极反应式为_______。
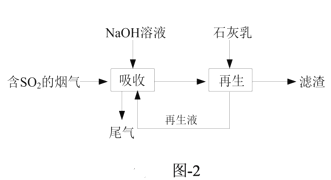
(3)钠钙双碱法可高效脱除烟气中的SO2,脱硫的流程如题图-2所示。
①“吸收”时气液逆流在吸收塔中接触,吸收时不宜直接使用石灰乳的原因是_______。

②水溶液中H2SO3、HSO![]() 、SO
、SO![]() 随pH的分布如题图3所示,“再生液”用NaOH溶液调pH至7~9得到溶液X,溶液X吸收SO2时主要反应的离子方程式为______。
随pH的分布如题图3所示,“再生液”用NaOH溶液调pH至7~9得到溶液X,溶液X吸收SO2时主要反应的离子方程式为______。
③已知Na2SO3的溶解度随着pH增大而减小。溶液X的pH对脱硫效率的影响如题图-4所示。当pH由6升高到7时,脱硫效率迅速增大的原因为______;当pH大于7时,随pH增大脱硫效率增速放缓的原因为______。

【答案】![]() B H2SO3 + 4e + 4H+ = S↓+ 3H2O 使用石灰乳会生成难溶的CaSO3,引起吸收塔堵塞 SO
B H2SO3 + 4e + 4H+ = S↓+ 3H2O 使用石灰乳会生成难溶的CaSO3,引起吸收塔堵塞 SO![]() + SO2 + H2O = 2HSO
+ SO2 + H2O = 2HSO![]() “再生液”中Na2SO3的浓度增大,吸收SO2的效率增强 随着pH进一步增大,“再生液”中Na2SO3的溶解度因pH增大而减小,Na2SO3会析出,Na2SO3浓度减小,脱硫效率增速放缓。
“再生液”中Na2SO3的浓度增大,吸收SO2的效率增强 随着pH进一步增大,“再生液”中Na2SO3的溶解度因pH增大而减小,Na2SO3会析出,Na2SO3浓度减小,脱硫效率增速放缓。
【解析】
利用盖斯定律进行计算,选择合适温度时,要使NH4HSO3的含量较多,二氧化硫和氨气的含量较少。根据化合价的变化写出电极反应式。二氧化硫会与石灰乳反应产物亚硫酸钙的溶解性分析。根据图像可以看出亚硫酸根的浓度在增大,写出亚硫酸根与二氧化硫反应的离子方程式。“再生液”中Na2SO3的浓度变化分析吸收效率的变化。根据Na2SO3的溶解度随着pH增大而减小分析。
(1)①2NH3(g) +H2O(l) +SO2(g) =(NH4)2SO3(aq) ΔH= akJ·mol1
②(NH4)2SO3(aq)+H2O(l) +SO2(g) =2NH4HSO3(aq) ΔH = bkJ·mol1
③2(NH4)2SO3(aq) +O2(g) =2(NH4)2SO4(aq) ΔH =ckJ·mol1
根据盖斯定律,将![]() (①-②+③),可得到反应NH3(g) +NH4HSO3(aq) +
(①-②+③),可得到反应NH3(g) +NH4HSO3(aq) +![]() O2(g) = (NH4)2SO4(aq)的ΔH=
O2(g) = (NH4)2SO4(aq)的ΔH=![]() kJ·mol1;
kJ·mol1;
实验结果如题图-1所示,为了尽可能获得NH4HSO3,则吸收塔合适的温度约为:温度在25℃是亚硫酸氢铵的量不多,31℃时亚硫酸氢铵的含量较多,氨气和二氧化硫的量较小,符合要求,35℃时亚硫酸氢铵的含量较多,氨气和二氧化硫的量较多,不符合要求,选择合适的温度是31℃,答案选B;
(2)H2SO3在阴极被还原为硫单质,硫元素的化合价从+4降低到0价,1molH2SO3失去4mol电子,阴极的电极反应式为H2SO3 + 4e + 4H+ = S↓+ 3H2O;
(3)①吸收二氧化硫时,不宜直接使用石灰乳的原因是:二氧化硫与石灰乳中的氢氧化钙反应生成亚硫酸钙,CaSO3属于难溶的物质,引起吸收塔堵塞;
② “再生液”用NaOH溶液调pH至7~9得到溶液X,主要含有亚硫酸钠,亚硫酸钠溶液吸收SO2生成亚硫酸氢钠,主要反应的离子方程式为:SO![]() + SO2 + H2O = 2HSO
+ SO2 + H2O = 2HSO![]() ;
;
③从图像可以看出,当pH由6升高到7时,亚硫酸钠溶液的浓度在增大,脱硫效率迅速增大的原因是“再生液”中Na2SO3的浓度增大,吸收SO2的效率增强;当pH大于7时,Na2SO3的溶解度随着pH增大而减小,亚硫酸钠会析出,亚硫酸钠浓度减小,随pH增大脱硫效率增速放缓。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】2份50mL同样的NaOH的溶液,分别向其中逐渐通入一定量的CO2,得到甲和乙 两种溶液,在甲和乙溶液中分别逐渐加入1mol/LHCl的盐酸溶液,产生的二氧化碳气体(标准状况)与所加入盐酸的体积之间的关系如图所示的关系。
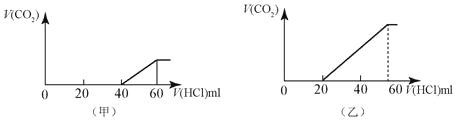
请回答下列问题:
(1)甲溶液中的溶质是____,其物质的量的比值是____。
(2)乙溶液中的溶质是____,其物质的量的比值是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)室温下,2g苯(C6H6)完全燃烧生成液态水和CO2,放出83.6kJ的热量,写出1molC6H6完全燃烧的热化学方程式:______。
(2)已知:Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s)△H=+akJmol-1;C(s)+O2(g)=CO2(g)△H=-bkJmol-1,则2Fe(s)+
CO2(g)+2Fe(s)△H=+akJmol-1;C(s)+O2(g)=CO2(g)△H=-bkJmol-1,则2Fe(s)+![]() O2(g)=Fe2O3(s)的△H=________。
O2(g)=Fe2O3(s)的△H=________。
(3)已知几种化学键的键能如表所示:
化学键 | Cl—Cl | F—F | Cl—F |
键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+3F2(g)![]() 2ClF3(g)的△H=_____________ kJ·mol-1。
2ClF3(g)的△H=_____________ kJ·mol-1。
(4)如图是乙烷、二甲醚燃烧过程中的能量变化图。
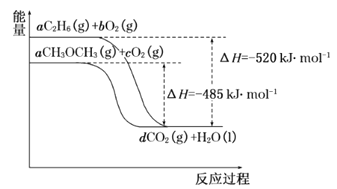
请回答下列问题:
①乙烷的燃烧热ΔH=_______kJ·mol-1。
②根据题图写出二甲醚完全燃烧时的热化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】19.2 g Cu加入到100 mL一定浓度的硝酸溶液中,假定两者恰好完全反应,同时产生标准状况下8.96 L NO和NO2的混合气体(忽略气体的溶解及转化)。求:
(1)混合气体中NO和NO2的体积比。_____________
(2)硝酸溶液的物质的量浓度。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理来解释的是( )
A.SO2氧化SO3,往往需要使用催化剂2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
B.500 ℃左右的温度比室温更有利于合成氮反应N2(g)+ 3H2 (g)![]() 2NH3(g) △H<0
2NH3(g) △H<0
C.H2、I2、HI平衡混合气体加压后颜色加深H2(g)+ I2(g)![]() 2HI(g)
2HI(g)
D.实验室采用排饱和食盐水的方法收集氯气Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喷泉实验是一种常见的自然现象,其产生原因是存在压强差。试根据如图,回答下列问题:
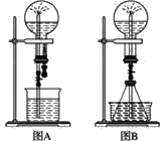
(1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是(________)
A.氯化氢和水
B.氯气和氢氧化钠溶液
C.氯化氢和汽油
D.二氧化碳和氢氧化钠溶液
(2)在图B的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是(________)
A.铜与稀盐酸
B.碳酸氢钠与氢氧化钠溶液
C.碳酸钙与稀硫酸
D.碳酸氢铵与稀盐酸
(3)在图B的锥形瓶外放一水槽,锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质不可能是(________)。
A.浓硫酸 B.生石灰
C.硝酸铵 D.烧碱
(4)比较图A和图B两套装置,以产生喷泉的原理来分析,图A是__上部烧瓶内压强;城市中常见的人造喷泉及火山爆发的原理与上述__(填“图A”或“图B”)装置的原理相似。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取SO2并验证SO2的某些性质的装置,请回答:

(1)在⑥中发生反应的化学方程式为______________________________________。
(2)①中的实验现象为石蕊溶液____________,此实验证明SO2具有____________的性质。
(3)②中的品红溶液________,证明SO2有________性。
(4)③中的实验现象是________________________,证明SO2有____________性。
(5)④中的实验现象是______,证明SO2有______性。
(6)⑤的作用是____________,反应的化学方程式为____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探索CO和NO2这类化合物的特征及反应机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
I.CO可以与H2反应制备合成天然气(SNG)。涉及反应如下:
CO甲烷化:CO(g)+3H2(g)CH4(g)+H2O(g)![]() 1=-206.2kJ·mol-1
1=-206.2kJ·mol-1
水煤气变换:CO(g)+H2O(g)CO2(g)+H2(g)![]() 2=-41.2kJ·mol-1
2=-41.2kJ·mol-1
(1)反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的![]() =_____kJ·mol-1。某温度下,分别在起始体积相同的恒容容器A、恒压容器B中加入1molCO2和4molH2的混合气体,两容器反应达平衡后放出或吸收的热量较多的是_____(填“A”或“B”)。
=_____kJ·mol-1。某温度下,分别在起始体积相同的恒容容器A、恒压容器B中加入1molCO2和4molH2的混合气体,两容器反应达平衡后放出或吸收的热量较多的是_____(填“A”或“B”)。
(2)在恒压管道反应器中将原料气H2和CO按一定比例通入,在催化剂作用下制备合成天然气,400℃、p总为100kPa时反应体系平衡组成如表所示。
组分 | CH4 | H2O | H2 | CO2 | CO |
体积分数 | 45.0 | 42.5 | 10.0 | 2.00 | 0.500 |
该条件下CO的总转化率α=______。若将管道反应器升温至500℃,反应达到平衡后CH4的体积分数![]() ______45.0%(填“>”、“<”或“=”)。
______45.0%(填“>”、“<”或“=”)。
II.NO2可发生二聚反应生成N2O4,化学方程式为2NO2![]() N2O4。该反应达到平衡后,升高温度可使体系颜色加深。
N2O4。该反应达到平衡后,升高温度可使体系颜色加深。
(3)已知该反应的正反应速率方程为υ正=k正·c2(NO2),逆反应速率方程为υ逆=k逆·c(N2O4),其中k正、k逆分别为正、逆反应的速率常数。则右图(lgk表示速率常数的对数;![]() 表示温度的倒数)所示①、②、③、④四条斜线中,能表示lgk正随
表示温度的倒数)所示①、②、③、④四条斜线中,能表示lgk正随![]() 变化关系的是斜线______,能表示lgk逆随
变化关系的是斜线______,能表示lgk逆随![]() 变化关系的是斜线______。
变化关系的是斜线______。

(4)图中A、B、C、D点的纵坐标分别为a+1.5、a+0.5、a-0.5、a-1.5,则T1温度时化学平衡常数K=______mol-1·L。已知T1温度时,某时刻恒容密闭容器中NO2、N2O4浓度均为0.2mol·L-1,此时υ正______υ逆(填>或<);该反应达到平衡后,若将温度从T1升高到T2重新达到平衡,则T1温度时平衡压强p(T1)______T2温度时平衡压强p(T2)(填“>”、“=”或“<”),原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
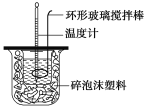
(1)写出该反应的热化学方程式(中和热为57.3 kJ·mol-1):_____。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
温度 实验次数 | 起始温度T1/℃ | 终止温度 T2/℃ | 温度差平 均值(T2 -T1)/℃ | ||
H2SO4 溶液 | NaOH 溶液 | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ___ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸溶液的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1。则中和热ΔH=____(取小数点后一位)。
③上述实验数值结果与57.3kJ·mol-1有偏差,产生偏差的原因可能是____(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com