
【题目】研究证明高铁酸钠(Na2FeO4) 是一种“绿色环保高效”消毒剂, 比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.用氯气和氢氧化钠溶液反应制备NaClO溶液
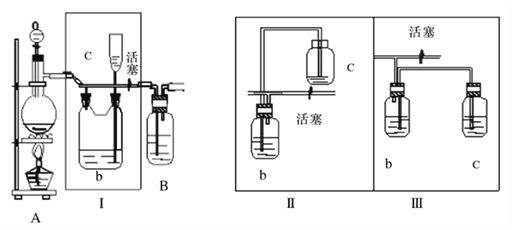
(1)A是氯气发生装置,写出实验室用此装置制取氯气的离子方程式__________。
(2)I装置的作用是__________ 。
(3)用图示的II或III代替I是否可行? __________。简要说明理由__________ 。
(4)将产生的氯气通入D装置中制NaClO溶液
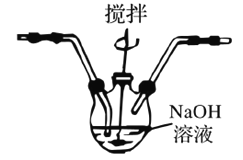
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
II.制备Na2FeO4
(1)将Fe(NO3)3溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是______。过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是__________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式__________。
【答案】 MnO2+4H++2C1- ![]() Mn2++Cl2↑+2H2O 收集并储存氯气 Ⅱ可行,Ⅲ不行 Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险,且由于B、C液差太小,不能使储存的Cl2全部排出 将D放在冷水中 2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH
Mn2++Cl2↑+2H2O 收集并储存氯气 Ⅱ可行,Ⅲ不行 Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险,且由于B、C液差太小,不能使储存的Cl2全部排出 将D放在冷水中 2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH
【解析】I. (1)①实验室用二氧化锰和浓盐酸加热反应生成氯化锰、氯气和水,离子方程式为:MnO2+4H++2C1- ![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
②从装置图可看出,I装置的作用是收集并储存氯气;
(3)比较装置Ⅰ、Ⅱ和Ⅲ发现,Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强会有危险,且由于B、C液差太小,不能使储存的Cl2全部排出。
(4) 温度过高会发生反应:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,所以为了防止产生NaClO3应将D放在冷水中。
5NaCl+NaClO3+3H2O,所以为了防止产生NaClO3应将D放在冷水中。
II. (1)Fe3+与在碱性条件下被ClO-氧化生成FeO42-本身被还原为Cl-,其反应的离子方程式是2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O;由于Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失,所以要用NaOH溶液溶解粗产品而不用水。因此,本题答案为:2Fe3++ 3C1O-+ 10OH-==2FeO42-+ 3Cl-+5H2O ;Na2FeO4在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失。
(2)负极是锌,失去电子在氢氧化钠的条件下生成氢氧化锌,高铁酸钠转化为氢氧化铁红褐色沉淀,电池反应为: 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH,因此,本题正确答案是: 3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如甲图所示(t0~t1阶段的c(B)变化未画出).乙图为t时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,t3~t4阶段为使用催化剂.下列说法中不正确的是
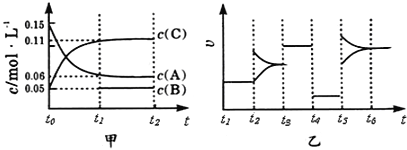
A. 若t1=15s,则用C的浓度变化表示的t0~t1段的平均反应速率为0.004molL-1s-1
B. t4~t5阶段改变的条件一定为减小压强
C. 该容器的容积为2L,B的起始物质的量为0.02mol
D. 该化学反应方程式为3A(g)B(g)+2C(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是 ( )
A.钢铁发生电化学腐蚀的正极反应式:Fe -2e- == Fe2+
B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- == 4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu -2e- == Cu2+
D.电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e-= Cl2 ↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D是形成化合物种类最多的元素。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为________;写出由甲制高聚物的反应方程式 。
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于________(“极性分子”或“非极性分子”);其电子式________;将乙加入浅绿色氯化亚铜溶液中,溶液变为棕黄色,写出该反应的离子方程式______________。
(3)写出B的基态原子电子排布图为 。与PH3相比,BA3易液化的主要原因是_____________;
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构。故B2C的空间构型是________,其为________(填“极性”或“非极性”)分子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池已经成为应用最广泛的可充电电池,某种锂离子电池的结构示意图如下,它在放电时有关离子转化关系如图所示,下列说法正确的是

A. Li+透过膜除允许Li+通过外,还允许H2O分子通过
B. 充电时,电池内部发生的总反应为Li++Fe2+![]() Li+Fe3+
Li+Fe3+
C. 充电时,钛电极与外电源的负极相连
D. 放电时,进入贮罐的液体发生的离子反应方程式为:S2O82-+Fe2+=Fe3++2SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子的2p能级有3个电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。回答下列问题:
(1)写出基态E+的价电子排布式:_________。基态A原子的第一电离能比B的大,其原因是__________。
(2)A5+由美国空军研究实验室推进科学与先进概念部Karl .O. Christed 于1999年成功合成,其结构呈‘V'形且该离子中各原子均达到8电子稳定结构,则A5+的结构式为________。
(3)B3分子的空间构型为______,其中B原子的杂化类型是______,与B3分子互为等电子体的微粒有_________(写一种离子)。
(4)向E的硫酸盐溶液中通入A的气态氢化物至过量,产生蓝色沉淀,随后沉淀溶解得到深蓝色溶液,向溶液中加入适量乙醇,析出蓝色晶体。加入乙醇的目的___________。 写出该配合物中配离子的结构简式__________。
(5)由长周期元素组成的镧镍合金、铜钙合金有相同类型的晶体结构XYn,它们有很强的储氢能力,其中铜钙合金的晶体的部分结构如图所示。
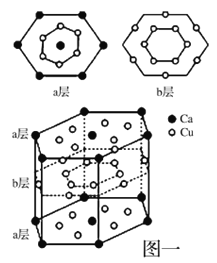
己知镧镍合金(LaNin)晶体中的重复结构单元如图一所示,该结构单元的体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶体空隙,体积不变),则LaNin中n=___ (填数值);氢在合金中的密度为_______g/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。

(1)往A溶液中分别滴入几滴KSCN溶液,溶液的颜色__________,
(2)根据上述过程写出有关反应的离子方程式:Fe3O4→A _________________,A→B ___________。
(3)向B溶液中加入NaOH溶液,可看到的现象是_______________________________________,此过程中发生的氧化还原反应化学方程式为__________________________________。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_______________胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________效应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一带路”为中国化工企业开辟了新的国际市场,能源环保是基础。在能源领域科学家提出构想——富集空气中的CO2,并使之与H2反应生成可再生能源甲醇.流程如下:
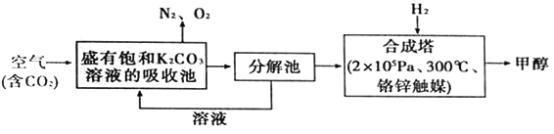
(1)在合成塔中,若有4400gCO2与足量H2完全反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式________________。
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2在不同催化剂作用下发生反应I、反应II、反应III,相同时间内CO2的转化率随温度变化如图1所示:
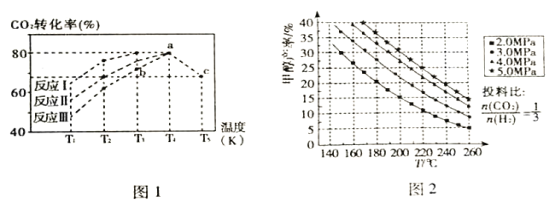
①催化效果最佳的反应是_________(填“反应I”、“反应II”、“反应III”)。
②b点反应速率v(正)______v(逆) (填“>”、“=”或“<”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是_________。
(3)选取合适的催化剂发生上述反应,测得甲醇的产率与反应温度、压强的关系如图2。
④分析图中数据可知,在220℃、5.0MPa时,CO2的转化率为________;将温度降低至140℃、压强减小至2.0MPa,CO2的转化率将_______(填“增大”、“减小”或“不变”)。
⑤200℃、2.0MPa时,将amol/LCO2和3amol/LH2充入VL密闭容器中,在催化剂作用下反应达到平衡。根据图中数据计算所得甲醇的质量______g(用含a、V的代数式表示)。
(4)用NaOH溶液吸收CO2所得饱和碳酸钠溶液可以对废旧电池中的铅膏(主要成分PbSO4)进行脱硫反应。已知Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,PbSO4(s)+CO32-(aq)==PbCO3(s)+SO42-(aq),则该反应的平衡常数K=___(保留三位有效数字);若在其溶液中加入少量Pb(NO3)2晶体,则c(SO42-):c(CO32-)的比值将_____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
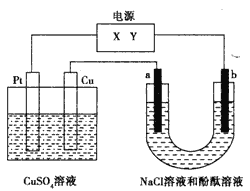
A. Pt为阴极,Cu为阳极
B. b极的电极反应式是2H++2e-=H2↑
C. 电解过程中CuSO4溶液的pH逐渐增大
D. Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com