
【化学——选修3:物质结构与性质】(15分)卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的______区;溴的价电子排布式为________________。
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是______。
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是______(写出名称)。
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图I、II所示:
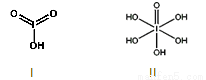
请比较二者酸性强弱:HIO3_____ H5IO6(填“>”、 “<”或“=”)。
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子。ClO2-中心氯原子的杂化轨道类型为________,写出一个ClO2-的等电子体__________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_________。

A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
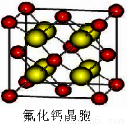
(7)已知CaF2晶体(见下图)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为___________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年宁夏银川一中高三第二次模拟考试 理综化学试卷(解析版) 题型:选择题
取一定质量的均匀固体混合物Cu、CuO和Cu2O,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20 g,另一份中加入500 mL稀硝酸(其还原产物为NO),固体恰好完全溶解,且同时收集到标准状况下NO气体4.48 L,则所用硝酸的物质的量浓度为
A.2.4 mol/L B.1.4 mol/L C.1.2 mol/L D.0.7 mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
在1升密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:(1)2A(g) 2B(g)+C(g);(2)A(g)
2B(g)+C(g);(2)A(g) C(g)+D(g)。当达到平衡时,测得c(A)=2.5 mol·L-1,c(C)=2.0 mol·L-1。则下列说法中正确的是:
C(g)+D(g)。当达到平衡时,测得c(A)=2.5 mol·L-1,c(C)=2.0 mol·L-1。则下列说法中正确的是:
A.达到平衡时A的总转化率为40%
B.达到平衡时c(B)为1.0 mol·L-1
C.达到平衡时c(B)=2c(D)
D.达到平衡时c(D)为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三第二次联考理综化学试卷(解析版) 题型:简答题
【化学–选修2:化学与技术】(15分)工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
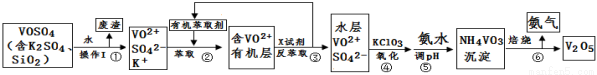
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),操作I的名称 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+2nHA(有机层) 2RAn(有机层)+nH2SO4 (水层)
2RAn(有机层)+nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)④的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 。
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有 和 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三第二次联考理综化学试卷(解析版) 题型:选择题
下列实验不合理的是:
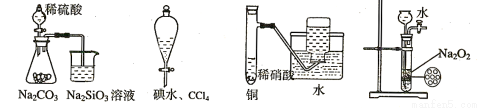
A.证明非金属性强弱 S>C>Si B.四氯化碳萃取碘水中的碘
C.制备并收集少量NO气体 D.制备少量氧气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三综合能力测试(五)理综化学试卷(解析版) 题型:选择题
原子序数依次增大的X、Y、Z、R、W、T六种前20号元素,X、Y原子的最外层电子数与其电子层数相等,Y、T位于同族,R最外层电子数是次外层的3倍,W无正价,甲的化学式为ZX3,是一种刺激性气味的气体,乙是由X、Z、W组成的盐。下列说法正确的是
A.由X、Z、W组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度
B.气态氢化物的稳定性:W<R< Z
C.原子半径:W <Z<Y,而简单离子半径:Y<Z<W
D.ZR2、TR2两化合物中R的化合价相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三二模考试理综化学试卷(解析版) 题型:填空题
[化学——选修3]物质结构与性质:(15分)有A、B、C、D、E五种元素。其相关信息如下:

请回答下列问题。
(1)写出E元素原子基态时M层的电子排布式 。
(2)C元素单质分子中含有δ和∏键的键数之比为 。
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是: :C2A4分子中c原子轨 道的杂化类型是 。
(4)A、C、E三种元素可形成:【E(CA3)4】2+配离子,其中存在的化学键类型有 (填序号):
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若【E(CA3)4】2+具有对称的空间构型.且当【E(CA3)4】2+中的两个CA3分子被两个Cl一取代时.能得到两 种不同结构的产物,则【E(CA3)4】2+的空间构型为 (填序号)。
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)B与D可形成离子化合物.其晶胞结构如图所示。其中D离子的配位数为 .若该晶体的密 度为a g·cm-3,则该晶胞中距离最近的B和D之间的距离是 cm(写出表达式即可,NA代表阿伏加得罗常数)
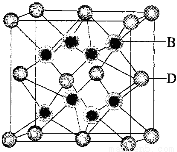
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:实验题
(15分)碱式碳酸钴 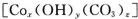 常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
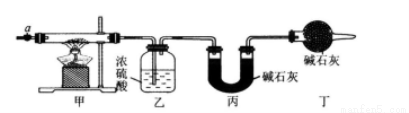
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中_______(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通人空气数分钟的目的是___________________________________.
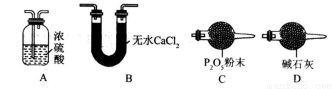
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_______(填字母)连接在_______(填装置连接位置)。
(4)若按正确装置进行实验,测得如下数据。
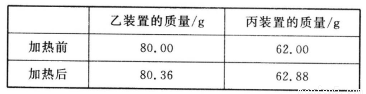
则该碱式碳酸钴的化学式为______________。
(5)含有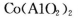 的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为_______。
的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为_______。
(6) 常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取
常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取 的一种工艺如下:
的一种工艺如下:

①净化除杂时,加入H2O2发生反应的离子方程式为____________________________.
②加入CoCO3 调pH为5.2~7.6,则操作1获得的滤渣成分为_____________________.
③加盐酸调整pH为2~3的目的为__________________________________________.
④操作Ⅱ过程为蒸发浓缩、______________(填操作名称)、过滤。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省金华十校高三下学期高考模拟(4月)理综化学试卷(解析版) 题型:选择题
化学与科学、社会、技术和环境密切相关。下列有关说法中错误的是
A.目前科学家已制得单原子层锗,其电子迁移率是硅的10倍,有望用于制造高能计算机芯片
B.2014年在西非国家爆发了埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
C.2014年德美科学家因开发超分辨荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代。利用此类光学显微镜可以观察活细胞内蛋白质等大分子
D.绿色化学期望利用化学原理从源头消除污染,在生产过程中充分利用原料,实现零排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com