
| A. | 氯化硼分子间含有氢键 | |
| B. | 氯化硼中心原子采用sp杂化 | |
| C. | 氯化硼分子呈正三角形,属非极性分子 | |
| D. | 其分子空间结构类似CH4O |
分析 氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,可知为分子晶体,且为平面正三角形,BCl3中B为不存在孤对电子,成键数为3,则B为sp2杂化,以此来解答.
解答 解:A.B的非金属性较弱,氯化硼分子间不含有氢键,故A错误;
B.BCl3中B为不存在孤对电子,成键数为3,则B为sp2杂化,故B错误;
C.分子中键与键之间的夹角为120°,可知氯化硼分子呈正三角形,结构对称,正负电荷的中心重合,属非极性分子,故C正确;
D.CH4O中C为四面体构型,氯化硼分子呈正三角形,空间结构不类似,故D错误;
故选C.
点评 本题考查杂化及分子构型,为高频考点,把握分子的性质及结构判断分子构型、原子杂化为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | H+、Fe2+、Cl-、NO3- | B. | NH4+、SO42-、Na+、OH- | ||
| C. | Cu2+、Fe3+、NO3-、Cl- | D. | H+、Na+、HCO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
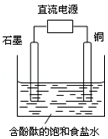 某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是( )| A. | 铜是电解池的阳极 | B. | 石墨电极附近溶液呈红色 | ||
| C. | 铜电极上产生的是无色气体 | D. | 石墨电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔 | B. | 乙烯 | C. | 丁二烯 | D. | 丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Z)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
| A. | 若使用催化剂,则反应速率和X的转化率均增大 | |
| B. | 其他条件不变,升高温度,再达到平衡时c(Z)=0.8 mol•L-1,则△H>0 | |
| C. | 其他条件不变,容器体积压缩到1.0 L,平衡常数将增大 | |
| D. | 温度不变,向容器中再充入2 mol X、1 mol Y,反应达到新平衡时 $\frac{n(Z)}{n(Y)}$ 增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 静电除尘器除去空气中的飘尘是利用胶体粒子的带电性而加以除去 | |
| B. | 溶液和胶体均为呈电中性的分散系 | |
| C. | FeCl3溶液和Fe(OH)3胶体的本质区别是后者可以产生丁达尔现象 | |
| D. | 由于胶粒之间的排斥作用,胶粒不易聚集成大的颗粒,所以胶体比较稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com