
| A. | 1mol任何物质都约含有6.02×1023个原子 | |
| B. | 物质的量为2mol的BaCl2中,含有Cl-个数为2NA | |
| C. | O2的摩尔质量是32 | |
| D. | 摩尔是物质的量的单位 |
分析 A.物质可能由原子、分子构成,且可能为多原子分子;
B.结合N=nNA及分子构成计算;
C.摩尔质量的单位为g/mol;
D.物质的量为基本物理量之一,其单位为摩尔.
解答 解:A.1mol由单原子构成的物质都约含有6.02×1023个原子,故A错误;
B.物质的量为2mol的BaCl2中,含有Cl-个数为4NA,故B错误;
C.O2的摩尔质量是32g/mol,故C错误;
D.物质的量为基本物理量之一,摩尔是物质的量的单位,故D正确;
故选D.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成、物质的量、微粒数的关系为解答关键,侧重分析与应用能力的考查,注意选项A为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 乙烯属于不饱和链烃,乙烷属于饱和链烃 | |
| B. | 乙烯分子中所有原子处于同一平面上,乙烷分子中的原子不在同一平面上 | |
| C. | 乙烯分子中的 双键比乙烷分子中的 C-C 单键更稳定,性质更活泼 | |
| D. | 乙烯能使酸性 KMnO4 溶液褪色,乙烷不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CBr2F2 | B. | CH3CH(OH)COOH | C. | CH3CH2CH3 | D. | CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
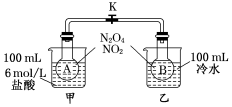 为测定温度对平衡的影响,设计了如下试验.
为测定温度对平衡的影响,设计了如下试验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
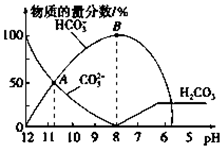 常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )
常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )| A. | 在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-) | |
| B. | 当溶液的pH为7时,溶液的总体积大于20mL | |
| C. | 在B点所示的溶液中,浓度最大的离子是HCO3- | |
| D. | 在0.1 mol•L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{2b-c}{a}$ | B. | $\frac{2b-c}{2a}$ | C. | $\frac{2b-c}{3a}$ | D. | $\frac{2b-c}{6}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | T | |
| L |
| A. | 原子半径:X<Y<Z<T<L | |
| B. | 气态氢化物的还原性:L>Z>T | |
| C. | 含x的两种盐溶液混合可能生成沉淀 | |
| D. | Y的含氧酸的酸性小于T的含氧酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com