
(14��)������ͼװ�ý���ľ̿�ۺ�Ũ����ķ�Ӧ�������ļ��顣
��֪���Ϻ�ɫ�����Ը��������Һ�������������������ԭ��Ӧ�������Ը�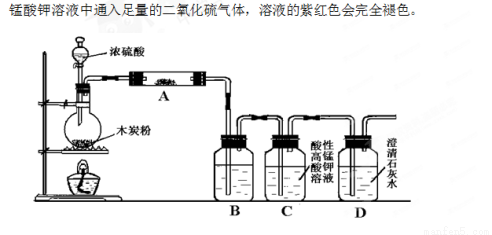
��1����װ������װ�ú�����Ҫ���еIJ����ǣ� ��
��2��д��Ũ�����ľ̿���ڼ��������·�����Ӧ�Ļ�ѧ����ʽ�� ��
��3����ͼ�е�װ�ü���������Ӧ��ȫ�����д������������ʾ��������Ӧ�����Լ������Ƽ������ã�A�м�����Լ��������� �� ��B�м�����Լ��������� �� ��
��4��ʵ��ʱ��C��Ӧ�۲쵽ʲô���ſ���˵�������˶�����̼�� ��
��ÿ��2�֣���14�֣���1�����װ�õ������ԡ���2��2H2SO4��Ũ��+C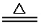 2SO2��+CO2��+2H2O
2SO2��+CO2��+2H2O

��������
�����������1�����й������ʵ���У���װ������֮���Ҫ���������Եļ�飻��2��̼��Ũ�����ڼ������������ɶ�����̼�����������ˮ����3���������������ˮ����ͭ��ĩ����ˮ������Ʒ����Һ�����������ȥ��������֮����ͨ������ʯ��ˮ���������̼����4��ֻ�ж���������ɾ��ˣ�����ʯ��ˮ����Dz���˵���ж�����̼���ɣ�����װ��ͼ������ֻ�����Ը��������ɫ���ʾ�����˵�����������ѳ��ɾ���
���㣺��Ӧ����ʽ����д�����ʵļ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�����ǰģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�˵����ȷ����
A�������£�0.1 mol��L��1 CH3COOH��Һ��pH=1
B��Ǧ�����ڷŵ�����У������������ӣ�����pH����
C����ӦCO2(g)+C(s)=2CO(g)�ڵ����²����Է����У������H��0
D�������£���AgCl��Һ�м�������NaCl������Һ����c(Ag+)��Ksp(AgCl)����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��һ��ѧ��5�¶ο���ѧ�����Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�������ȷ�Ӧ����
A��ʯ��ʯ�ڸ����µķֽⷴӦ B����ʯ�Һ�ˮ�ķ�Ӧ
C������������������Һ�ķ�Ӧ D��ľ̿��������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�⽭�и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£��� 0.1 mol��L��1HCl��Һ�ζ�10.0 mLŨ��Ϊ0.1 mol��L��1 Na2CO3��Һ�����õζ�������ͼ��ʾ������˵����ȷ����

A����V��0ʱ��c(H��)��c(HCO 3��)��c(H2CO3)��c(OH��)
B����V��5ʱ��c(CO32��)��c(HCO 3��)��c(H2CO3)��2c(Cl��)
C����V��10ʱ��c(Na��)��c(HCO 3��)��c(CO32��)��c(H2CO3)
D����V��aʱ��c(Na��)��c(Cl��)��c(H��)��c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�⽭�и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ȼ�ϵ����ȼ�ϣ�����CO��H2��CH4�ȣ��������������Ӧ�����˷�Ӧ�Ļ�ѧ��ת��Ϊ���ܵ�װ�ã������ͨ����KOH��Һ�����й��ڼ���ȼ�ϵ�ص�˵������ȷ����
A��������ӦʽΪCH4+10OH--8e=CO32-+7H2O
B��������ӦʽΪO2+2H2O+4e=4OH-
C�����Ų��Ϸŵ磬�������Һ���Բ���
D������ȼ�ϵ�ص����������ʱȼ���ȼ�յ����������ʴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�⽭�и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��8�֣����Т�BaCl2 �� �ڽ��ʯ �� ��NH4Cl �� ��Na2SO4 �� �ݸɱ� ���� �߶������辧���������ʣ�������Ҫ��ش𣨽����ʵ�����������пո��У���
��1������ԭ�Ӿ���Ļ�������_____________��
��2����̬ʱ���ڷ��Ӿ������____________��
��3���ۻ�ʱ��Ҫ�ƻ����ۼ�����___________���۵���͵���___________��
��4���Ⱥ������Ӽ��ֺ��й��ۼ�����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�⽭�и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��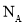 ��ʾ�����ӵ�������ֵ������������ȷ����
��ʾ�����ӵ�������ֵ������������ȷ����
A��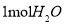 �к��е�ԭ����Ϊ
�к��е�ԭ����Ϊ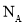
B��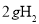 �к��е���ԭ����Ϊ2
�к��е���ԭ����Ϊ2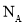
C�����³�ѹ�£�11.2L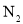 �к��еķ�����Ϊ0.5
�к��еķ�����Ϊ0.5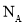
D��1L0.1mol��L-1NaNO3��Һ�к��е���������Ϊ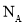
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��ͨ�и��������ε��в��Ի�ѧ�Ծ��������棩 ���ͣ������
��15�֣�5-��-2,3-����-1-��ͪ�Ǻϳ���ũҩ���������Ҫ�м��塣
��֪��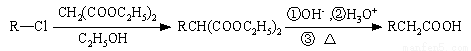
�Ի�����A������ʽΪC7H7Cl��Ϊԭ�Ϻϳ�5-��-2,3-����-1-��ͪ��������F�������������£�
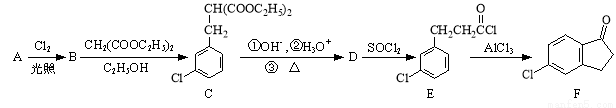
��д����ӦA��B�Ļ�ѧ����ʽ�� ��
�ƻ�����F�к��������ŵ�����Ϊ ����ӦB��C������Ϊ ��
��ij��������D��ͬ���칹�壬��ʹFeCl3��Һ����ɫ���ҷ�����ֻ��3�ֲ�ͬ��ѧ�������⡣д���û�����Ľṹ��ʽ�� (��дһ��)��
��E��F��ת���У������һ����F��Ϊͬ���칹��ĸ������ṹ��ʽΪ ��
�ɸ�������֪ʶ����������Ϣ��д���Ի�����F��CH2(COOC2H5)2Ϊ�л���Ӧԭ���Ʊ�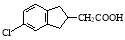 �ĺϳ�·������ͼ(ע����Ӧ����)���ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ(ע����Ӧ����)���ϳ�·������ͼʾ�����£�
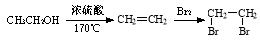
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�Ͼ��и�һ��ѧ����ĩѧ����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij������FeCl3��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·������С��Ϊȷ��������ķ�Һ����ɣ���������ʵ�飺��1��ȡ10mL��Һ����������AgNO3��Һ�����ɳ��� 8.61g����2����ȡ10mL��Һ����ͭƬ��ַ�Ӧ��ͭƬ����������0.256g�����й���ԭ��Һ��ɵ��ж���ȷ����
A��c(Cu2+) = c(Fe 2+)
B��c(Fe 2+)+ c(Cu2+)+ c(Fe 3+)= c(Cl��)
C��c(Cu2+)+c(Fe 3+) = 1.4 mol / L
D��c(Fe 3+) + c(Fe 2+) = 6 mol / L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com