
标准状况下,气态分子断开1mol化学键的焓变称为键焓。已知H—H,H—O,和O==O键的键焓△H分别为436KJ/mol,463KJ/mol,495KJ/mol,下列热化学方程式正确的是( )
A、H2O(g)==H2(g)+1/2O2( g) △H =—485KJ/mol
g) △H =—485KJ/mol
B、H2O(g)==H2(g)+1/2O2(g) △H = + 485KJ/mol
C、2 H2(g) + O2(g)==2 H2O(g) △H = + 485KJ/mol
D、2 H2(g) + O2(g)==2 H2O(g) △H =—485KJ/mol
科目:高中化学 来源: 题型:
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。 回答下列问题:
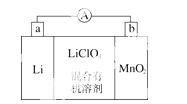
(1)外电路的电流方向是由________极流向________极。(填字 母)
母)
(2)电池正极反应式为__________________________。
(3)是否可用水代替电池中的混合有机溶剂?________(填“是”或“否”),
原因是________________________________________________。
(4)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为
____________________________________。K2MnO4在酸性溶液中歧化,生成KMnO2和MnO2的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2气体,放出890.3 kJ的热量。下列热化学方程式书写正确的是( )。
A.2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ·mol-1
B.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
D.CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
CH2=CH—CH=CH2(g) + 2H2(g) → CH3CH2CH2CH3(g) + 236.6 kJ
CH3-C≡C-CH3(g) + 2H2(g) → CH3CH2CH2CH3(g) + 272.7 kJ
由此不能判断
A.1,3-丁二烯和2-丁炔稳定性的相对大小
B.1,3-丁二烯和2-丁炔分子储存能量的相对高低
C.1,3-丁二烯和2-丁炔相互转化的热效应
D.一个碳碳叁键的键能与两个碳碳双键键能之和的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酸是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指现将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5O SO3H),再水解生成乙醇,写出相应反应的化学方程式__________________________________。
SO3H),再水解生成乙醇,写出相应反应的化学方程式__________________________________。
(2)已知:
甲醇脱水反应 2CH3OH(g)==CH3OCH3(g)+ H2O (g) 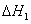 =
=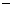 23.9 KJ﹒mol-1
23.9 KJ﹒mol-1
甲醇制烯烃反应 2CH3OH(g)== C2H4(g)+ 2H2O (g) 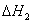 =
=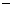 29.1 KJ﹒mol-1
29.1 KJ﹒mol-1
乙醇异构化反应 C2H5OH (g) ==CH3OCH3(g)
(g) ==CH3OCH3(g) 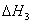 =+50.7KJ﹒mol-1
=+50.7KJ﹒mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)==C2H5OH(g)的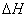 =______KJ﹒mol-1。与间接水合法相比,气相直接水合法的优点是____________________________________。
=______KJ﹒mol-1。与间接水合法相比,气相直接水合法的优点是____________________________________。
(3)下图为气相直接水合法乙烯的平衡转化率与温度、压强的关系(其中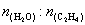 =1:1)
=1:1)
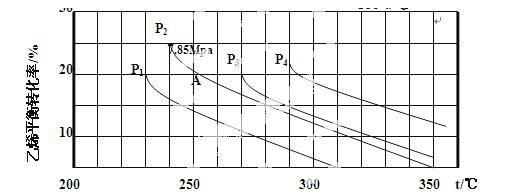
①列式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②图中压强(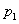 、
、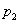 、
、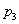 、
、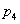 )的大小顺序为_________,理由是_________。
)的大小顺序为_________,理由是_________。
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9MPa,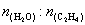 =0.6:1,乙烯的转化率为5%,若要进一步提高转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有_________、_________。
=0.6:1,乙烯的转化率为5%,若要进一步提高转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有_________、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2Zn(s)+O2(g)===2ZnO(s) ΔH=-701.0 kJ·mol-1 2Hg(l)+O2(g)== =2HgO(s) ΔH=-181.6 kJ·mol-1则反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的ΔH为( )
=2HgO(s) ΔH=-181.6 kJ·mol-1则反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的ΔH为( )
A.+519.4 kJ·mol-1 B.+259.7 kJ·mol-1
C.-259.7 kJ·mol-1 D.-519.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、R五种短周期非金属主族元素在元素周期表中的位置如图所示,下列有关说法正确的是( )
| X | Y | ||
| Z | W | R |
A.Z位于第三周期ⅤA族
B.X、Y的气态氢化物的稳定性:X>Y
C.原子半径大小顺序:Z>W>Y
D.W、R的最高价氧化物对应水化物的酸性:W>R
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com