
| A、Na+、K+、Cu2+、SO42- |
| B、NH4+、Na+、NO3-、Cl- |
| C、K+、Ca2+、HCO3-、Cl- |
| D、Mg2+、Na+、Cl-、OH- |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料 |
| C、二氧化硅是制造玻璃的主要原料 |
| D、自然界中硅元素贮量丰富 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、露天焚烧垃圾 |
| B、用煤火力发电 |
| C、开发利用太阳能 |
| D、乱砍滥伐树木 |
查看答案和解析>>
科目:高中化学 来源: 题型:
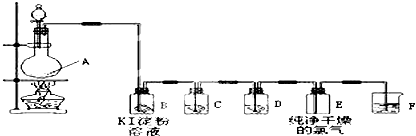
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应速率可用于衡量化学反应进行的快慢 |
| B、化学反应的限度不可改变 |
| C、可逆反应达到化学平衡状态时,正、逆反应速率均为零 |
| D、增大反应物浓度或升高反应温度都能增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com