
某混合液中含有等物质的量的CuSO4、FeSO4、Fe2(SO4)3。已知下表数据:
物质(25℃) | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
完全沉淀时的pH | ≥6.4 | ≥9.6 | 3~4 |
下列叙述正确的是
A.混合溶液中:c(SO42-):[ c(Cu2+) +c(Fe3+) +c(Fe2+)]=5:4
B.若向混合溶液中加入铁粉,不可能观察到红色固体析出
C.若向混合溶液中加入足量氯水,调节pH到3~4后过滤,得到纯净的CuSO4溶液
D.若向混合溶液中逐滴加入烧碱溶液,首先生成Fe(OH)3沉淀
D
【解析】
试题分析:A、设各物质的物质的量浓度均是1mol/L,则混合溶液中:c(SO42-)=1+1+3=5mol/L,c(Cu2+) +c(Fe3+) +c(Fe2+)=1+1+2=4mol/L,但金属阳离子水解使总浓度小于4mol/L,所以c(SO42-):[ c(Cu2+) +c(Fe3+) +c(Fe2+)]>5:4,错误;B、向混合液中加入铁粉,铁先与铁离子反应生成亚铁离子,若铁有剩余,则铁与铜离子反应生成铜单质,所以可能观察到红色固体析出,错误;C、若向混合溶液中加入足量氯水,亚铁离子转化为铁离子,调节pH到3~4后铁离子完全沉淀,过滤,此时溶液中存在铜离子、氯离子、硫酸根离子,所以不可能得到纯净的CuSO4溶液,错误;D、根据阳离子沉淀的pH可知,向溶液中滴入氢氧化钠溶液时,铁离子先沉淀生成氢氧化铁,正确,答案选D。
考点:考查氧化还原反应的顺序的判断,水解应用,离子沉淀的分析判断


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
向l mL 0.5mol·L-1AlCl3溶液中加入3 mL饱和NaF溶液,再加入l mL 3mol·L-1氨水,没有生成白色沉淀,其最主要的原因是
A.3mol·L-1氨水的浓度不够大,溶液的碱性不够强
B.NaF溶液碱性较强,Al3+完全反应生成AlO2-,而AlO2-不能与氨水反应生成Al(OH)3
C.氨水为弱碱溶液,Al3+不与弱碱反应
D.Al3+与F-结合生成新物质,溶液中几乎没有Al3+
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三11月阶段模块考试化学试卷(解析版) 题型:选择题
现将1mo1Cu2S与144克FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2 、CuSO4的混合溶液,并产生NO气体。则最终反应所得NO物质的量为
A.4 mo1 B.5 mo1 C.6 mo1 D.7 mo1
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三11月阶段模块考试化学试卷(解析版) 题型:选择题
“化学是一门中心学科,与社会、生活、科研密切的关系”。下列叙述中,不正确的是
A.大量使用燃煤发电是形成雾霾的主要原因
B.天然气、煤气大量泄漏遇到明火会爆炸
C.利用化学反应可实现12C到14C的转化
D.晶体硅可用于光伏发电、制造芯片
查看答案和解析>>
科目:高中化学 来源:2015届山东省乐陵市高三10月初检测化学试卷(解析版) 题型:选择题
下列各组中的实验步骤及现象,能达到相应实验目的的是
| 实验目的 | 实验步骤及现象 |
A | 检验亚硫酸钠试样是否变质 | 试样 |
B | 制取氯气并探究氯气是否具有漂白性 | MnO2和稀盐酸 |
C | 证明酸性条件H2O2氧化性比I2强 | 碘化钠溶液 |
D | 探究浓度对于化学平衡的影响 | FeCl3和KSCN混合溶液 |
查看答案和解析>>
科目:高中化学 来源:2015届山东省乐陵市高三10月初检测化学试卷(解析版) 题型:选择题
下列有关物质分类或归类中,正确的是
①混合物:盐酸、漂白粉、氯水、水银 ②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、石膏、冰醋酸、氯化银 ④同素异形体:C60、C70、金刚石、石墨
A.只有①③ B.只有②③ C.只有③④ D.只有④
查看答案和解析>>
科目:高中化学 来源:2015届山东省临沂市高三10月份月考化学试卷(解析版) 题型:实验题
无水氯化铝是一种重要的化工原料,利用明矾石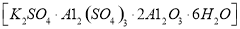 制备无水氯化铝的流程如下:
制备无水氯化铝的流程如下:
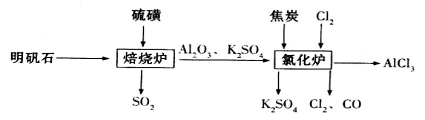
(1)验证焙烧炉产生的气体含有SO2的方法是________________________________。
(2)吸收焙烧炉中产生的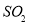 ,下列装置合理的是________(填代号)。
,下列装置合理的是________(填代号)。
(3)氯化炉中发生反应的化学方程式为_________________________________________。
(4)生产氯化铝的过程中产生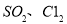 等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要描述实验步骤、现象和结论)____________。
等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要描述实验步骤、现象和结论)____________。
仪器自选;可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
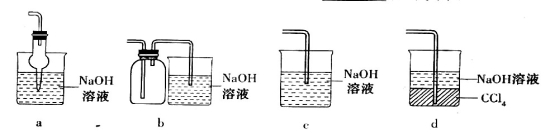
(5)某学习小组设计用如下装置验证二氧化硫的某些化学性质。

①能说明二氧化硫具有氧化性的实验现象为_____________________________________。
②写出a瓶中发生反应的离子方程式___________________________________________。
③充分反应后,取a瓶中的溶液分成三份,分别进行如下实验。
实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色
实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去
实验III:向第三份溶液中加入BaC12溶液,生成白色沉淀
上述实验中能证明二氧化硫具有还原性的是________(填实验代号)。
查看答案和解析>>
科目:高中化学 来源:2015届山东省临沂市高三10月份月考化学试卷(解析版) 题型:选择题
下列有关结构和性质的说法正确的是
A.元素铯的两种核素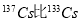 多4个质子
多4个质子
B.P、S、C1得电子能力和最高价氧化物对应水化物的酸性均依次增强
C.元素原子的最外层电子数越多,越容易得电子
D.从上到下,第VIIA族元素氢化物的热稳定性和还原性均依次减弱
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列有机物中,能发生消去反应生成2种烯烃,又能发生水解反应的是
A.2-甲基-2-氯丙烷 B.2-甲基-3-氯戊烷
C.2,2-二甲基-1-氯丁烷 D.1,3-二氯苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com