
【题目】室温下,某溶液中由水电离产生的c(H+)等于10-10mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4 B.NaCl
C.HCl D.Ba(OH)2
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-的物质的量浓度与200mL1 mol/L BaCl2溶液中Cl-的物质的量浓度相同的是
A. 100 mL 2 mol/L MgCl2溶液 B. 200 mL 2 mol/L NaCl溶液
C. 250 mL 1 mol/L AlCl3溶液 D. 100 mL 2 mol/L KClO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图只表示出与反应有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气体,请写出下列空白。

(1)化合物W的化学式可能是 或 ,C的电子式 ,F的颜色 。
(2)反应③的离子方程式为 。
(3)反应②中氧化剂和还原剂的物质的量之比为 。
(4)写出A→E的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298 K、100 kPa条件下:
①4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2 834.9 kJ·mol-1
②4Al(s)+2O3(g)===2Al2O3(s) ΔH=-3 119.1 kJ·mol-1
由此得出的正确结论是( )
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量低,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应
D.O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,金属元素与非金属元素分界线附近,能找到( )
A. 制半导体材料的元素
B. 制农药的元素
C. 制催化剂的元素
D. 制耐高温合金的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是
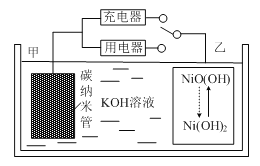
A.放电时,甲电极为正极,OH-移向乙电极
B.放电时,乙电极反应为:
NiO(OH)+H2O+e-=Ni(OH)2+OH-
C.充电时,电池的碳电极与直流电源的正极相连
D.电池总反应为H2+2NiOOH![]() 2Ni(OH)2
2Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中少量杂质所需除杂试剂及方法不正确的是
物质(杂质) | 除杂试剂 | 除杂方法 | |
A | 乙醇(水) | CaO | 蒸馏 |
B | 淀粉溶液(NaCl) | ——— | 渗析 |
C | CO2(HCl) | NaOH溶液 | 洗气 |
D | NaCl溶液(I2) | CCl4 | 萃取分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定质量的稀盐酸中加入镁粉至过量,下图中横坐标表示镁粉的质量,则纵坐标表示 ( )

A.溶液的质量 B.稀盐酸的质量
C.氯化镁的质量 D.生成气体的质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下图:
有关氢氧化物开始沉淀和沉淀完全的pH如下表:

氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
问答下列问题:
(1) 酸浸前将碳酸锰矿粉碎的作用是 。
(2) 酸浸后的溶液中含有Mn2+、SO42-,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其反应的离子方程式为 。
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是 。
③加入BaS,除去Cu2+、Pb2+后,再加入NaF溶液,除去 。
(3) 从溶液A中回收的主要物质是 ,该物质常用作化肥。
(4) MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com