
下列递变情况中正确的是
A.HF、HCl、HBr、HI的沸点依次升高
B.HF、HCl、HBr、HI还原性依次增强
C.HF、HCl、HBr、HI稳定性依次增强
D.HF、HCl、HBr、HI酸性依次增强
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:2016届黑龙江省高三第三次模拟理综化学试卷(解析版) 题型:选择题
已知X、Y、Z、W、R五种元素,原子序数依次增大,且原子序数都小于20,X元素的原子是所有元素中原子半径最小的,Y、W同主族,Z、W同周期,Y元素原子的最外层电子数是次外层的3倍,Z、R是同周期中金属性最强的元素。下列说法不正确的是( )
A.原子半径:X<Y<Z<W<R
B.由X、Y、Z、W四种元素组成的化合物既含有共价键又含离子键
C.沸点:X2Y>X2W
D.Y与W形成的化合物WY2是形成酸雨的主要物质之一
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:实验题
钒是一种熔点很高的金属,具有良好的可塑性和低温抗腐蚀性,有延展性、硬度大,无磁性。广泛应用于钢铁、航空航天、能源、化工等领域。中铝集团 (平果铝业公司)目前使用一种新型工艺,以便从铝业生成的固体废料——赤泥中提取金属钒,具体工艺流程图如下:

已知:
I.钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,存在平衡
VO2+ +H2O VO3- +2H+。
VO3- +2H+。
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
物质 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 难溶 | 难溶 | 易溶 |
Ⅲ.部分离子的沉淀pH值:
Cu2+ | Fe2+ | Fe3+ | |
开始沉淀pH值 | 5.2 | 7.6 | 2.7 |
完全沉淀pH值 | 6.4 | 9.6 | 3.7 |
请回答下列问题:
(1)碱浸步骤中最好选用 。
A.NaOH溶液 B.氨水 C.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式 。
(3)磁选步骤得到的磁性产品为 。
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使 。
(5)滤渣3的主要成分为 ,工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省等四校高三联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法正确的是
A.4.6 g NO2与N2O4的混合气体中所含氮原子数为0.1NA
B.常温常压下1.6 g甲烷所含共用电子对数为0.1NA
C.标准状况下,6.72 L CO2与足量Na2O2反应转移电子数为0.6NA
D.50 mL 98%浓硫酸(密度为1.84 g•cm-3)与足量铜共热,转移的电子数为 0.92NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
关于原子结构、元素性质的说法正确的是
A.非金属元素组成的化合物中只含共价键
B.IA族金属元素是同周期中金属性最强的元素
C.元素的原子均有相同的质子数和中子数
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
下列反应过程中,同时有离子键、极性共价键和非极性共价键断裂和形成的是
A.NH4Cl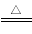 NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O=NH4HCO3
C.2NaOH+Cl2=NaCl+NaClO+H2O
D.2Na2O2+2CO2=2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
一种微粒的质子数和电子数分别与另一种微粒的质子数和电子数相同,则下列说法中错误的是
A.可能是不同的分子与原子
B.可能是不同的离子
C.可能是一种离子和一种分子
D.可能是某位素的同位素原子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
如图所示,a、b、c均为非金属单质,d、e均为含有10哥电子的共价化合物,,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )

A.常温下,单质a呈气态 B.单质c具有强氧化性
C.稳定性:d>e D.f受热易分解为d和e
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
下列关于物质性质的比较,不正确的是 ( )
A.酸性强弱:HIO4>HBrO4>HClO4 B.原子半径大小:Al>P>N
C.碱性强弱:KOH>NaOH>LiOH D.金属性强弱:Na>Mg>Al
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com