
·ÖĪö £Ø1£©½šŹōĄė×Ó»ÆŗóĶعżČŪŃĪĒØŅʵ½Õż¼«²¢ÓėÕż¼«½šŹōŗĻ½š»Æ£¬ĖµĆ÷øŗ¼«Ź§µē×ÓÉś³ÉµÄ½šŹōĄė×ÓŌŚÕż¼«µĆµē×ÓÉś³É½šŹōµ„ÖŹ£»
£Ø2£©¢ŁĢąŌŖĖŲŹōÓŚµŚĪåÖÜĘŚµŚ¢õA×壻
¢Ś¹¤ŅµČż·Ļ°üĄØ·ĻĘų”¢·ĻĖ®£Ø·ĻŅŗ£©”¢·ĻŌü£»
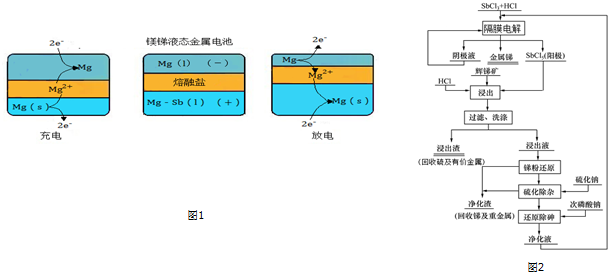
¢Ū“ÓĮ÷³ĢĶ¼ÖŠæÉŅŌ擳öŃō¼«²śĪļĪŖSbCl5£¬¶ųµē½āĶź³Éŗó²śÉś½šŹōĢą£¬Ó¦ĪŖSb3+Ąė×ÓŌŚŅõ¼«µĆµē×ÓÉś³É£»
¢Üøł¾ŻĮ÷³ĢĶ¼æ“³ö”°½ž³ö”±²½Öč»ŌĢąæóÓėŃō¼«²śĪļSbCl5·“Ó¦²śÉś²»ČÜĪļ£¬SbCl5¾ßÓŠŃõ»ÆŠŌ£¬Sb2S3¾ßÓŠ»¹ŌŠŌ£¬·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ŌŚ½ž³öŅŗÖŠŗ¬ÓŠĮņµ„ÖŹ£¬ĖłŅŌŃõ»Æ²śĪļÖŠÓŠĮņ£»
¢ŻCu2+øÕŗĆĶźČ«³ĮµķŹ±c£ØCu2+£©=1”Į10-5£¬øł¾ŻKsp£ØCuS£©=c£ØCu2+£©”Įc£ØS2-£©=8”Į10-45¼ĘĖć³öc£ØS2-£©£»
¢ŽøĆ·“Ó¦ÖŠAsCl3ĪŖŃõ»Æ¼Į£¬±»»¹ŌĪŖAsµ„ÖŹ£»Na3PO2ĪŖ»¹Ō¼Į£¬±»Ńõ»ÆĪŖH3PO3£»HClĻŌĖįŠŌ£¬Ģį¹©ĖįŠŌ»·¾³£¬øł¾ŻµĆŹ§µē×ÓŹŲŗćÅäĘ½£®
½ā“š ½ā£ŗ£Ø1£©øŗ¼«Ź§µē×ÓÉś³ÉµÄ½šŹōĄė×ÓŌŚÕż¼«µĆµē×ÓÉś³É½šŹōµ„ÖŹ£¬øŗ¼«½šŹōĪŖĆ¾£¬¹ŹÕż¼«µē¼«·“Ó¦Ź½ĪŖMg2++2e-=Mg£»
¹Ź“š°øĪŖ£ŗMg2++2e-=Mg£»
£Ø2£©¢ŁĢąŌŖĖŲŹōÓŚµŖ×åŌŖĖŲ£¬Ī»ÓŚÖÜĘŚ±ķÖŠµŚĪåÖÜĘŚµŚ¢õA×壻
¹Ź“š°øĪŖ£ŗµŚĪåÖÜĘŚµŚVA×壻
¢Ś¹¤ŅµČż·Ļ°üĄØ·ĻĘų”¢·ĻĖ®£Ø·ĻŅŗ£©”¢·ĻŌü£»
¹Ź“š°øĪŖ£ŗ·ĻĘų”¢·ĻĖ®£Ø·ĻŅŗ£©”¢·ĻŌü£»
¢Ū“ÓĮ÷³ĢĶ¼ÖŠæÉŅŌ擳öŃō¼«²śĪļĪŖSbCl5£¬¶ųµē½āĶź³Éŗó²śÉś½šŹōĢą£¬¹ŹŅõ¼«·“Ó¦Ź½ĪŖSb3++3e-=Sb£»
¹Ź“š°øĪŖ£ŗSb3++3e-=Sb£»
¢ÜŌŚ½ž³ö²½ÖčÖŠ¾ßÓŠŃõ»ÆŠŌµÄSbCl5ŗĶ¾ßÓŠ»¹ŌŠŌµÄSb2S3·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³É²»ČÜŠŌµÄSµ„ÖŹŗĶSbCl3£¬¹Ź·“Ó¦·½³ĢŹ½ĪŖSb2S3+3SbCl5=5SbCl3+3S£»
¹Ź“š°øĪŖ£ŗSb2S3+3SbCl5=5SbCl3+3S£»
¢ŻCu2+øÕŗĆĶźČ«³ĮµķŹ±c£ØCu2+£©=1”Į10-5£¬ÓÉKsp£ØCuS£©=c£ØCu2+£©”Įc£ØS2-£©£¬ÖŖc£ØS2-£©=$\frac{Ksp£ØCuS£©}{c£ØS{\;}^{2-}£©}$=$\frac{8”Į10{\;}^{-45}}{1”Į10{\;}^{-5}}$=8”Į10-40£»
¹Ź“š°øĪŖ£ŗ8”Į10-40£»
¢Ž“ĪĮ×ĖįÄĘ£ØNa3PO2£©×ö»¹Ō¼Į£¬±»Ńõ»ÆĪŖH3PO3£¬PŌŖĖŲÓÉ+1¼Ū±äĪŖ+3¼Ū£¬¼ŪĢ¬Éżøß2£»AsCl3±»»¹ŌĪŖAsµ„ÖŹ£¬AsŌŖĖŲÓÉ+3¼Ū±äĪŖ0¼Ū£¬¼ŪĢ¬½µµĶ3£¬ĖłŅŌAsCl3ŗĶNa3PO2ĻµŹżĪŖ2£ŗ3£¬øł¾ŻŌŖĖŲŹŲŗćÅäĘ½»Æѧ·“Ó¦·½³ĢŹ½ĪŖ2AsCl3+3Na3PO2+3HCl+3H2O=2As”ż+3H3PO3+9NaCl£®
¹Ź“š°øĪŖ£ŗ2£»3£»3£»3£»2£»3£»9£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌµē³ŲŗĶµē½ā³ŲµÄ¹¤×÷ŌĄķ¼°Ó¦ÓĆ£¬ĪļÖŹ·ÖĄėŗĶĢį“æµÄ·½·ØŗĶ»ł±¾²Ł×÷Ó¦ÓƵČÄŚČŻ£¬æ“×¼Į÷³ĢĶ¼ŹĒ½āĢāµÄ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗĻ³É°±Ź¹ÓĆøßŃ¹ | B£® | ÖĘĻõĖįÓĆPt-RhŗĻ½š×÷“߻ƼĮ | ||
| C£® | ÖĘĮņĖįŹ±½Ó“„ŹŅŹ¹ÓĆ½ĻøßĪĀ¶Č | D£® | ŗīŹĻÖĘ¼ī·ØŃ»·ĄūÓĆÄøŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 11.2g | B£® | 5.6g | C£® | 2.8g | D£® | 1.4g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹¤ŅµÉĻÓĆFeCl3ČÜŅŗĪüŹÕ·ĻĘųÖŠµÄH2SĘųĢ壬Ąė×Ó·½³ĢŹ½ĪŖ£ŗFe3++H2S=Fe2++S”ż+2H+ | |
| B£® | ŌŚ0.1 mol/LµÄAlCl3ČÜŅŗÖŠ£¬Na+”¢K+”¢SO42-”¢HCO3-¾łæÉ“óĮæ¹²“ę | |
| C£® | ³£ĪĀĻĀpH=4µÄNaHC2O4ČÜŅŗÖŠ£ŗc£ØH2C2O4£©£¾c£ØC2O42-£© | |
| D£® | ŅŃÖŖ25”ꏱNH4CNČÜŅŗĻŌ¼īŠŌ£¬Ōņ25”ꏱµÄµēĄėĘ½ŗā³£ŹżK£ØNH3•H2O£©£¾K£ØHCN£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 25”ꏱ£¬Ļņ100mL 0.1mol•L-1 NH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1mol•L-1 NaOHČÜŅŗ£¬µĆµ½µÄČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼£ØH2SO4ŹÓĪŖ¶žŌŖĒæĖį£©£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
25”ꏱ£¬Ļņ100mL 0.1mol•L-1 NH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1mol•L-1 NaOHČÜŅŗ£¬µĆµ½µÄČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼£ØH2SO4ŹÓĪŖ¶žŌŖĒæĖį£©£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | aµćŹ±ČÜŅŗµÄpH£¼1 | |
| B£® | cµćŹ±Ąė×ÓÅØ¶Č“óŠ”Ė³ŠņĪŖ£ŗc£ØNa+£©£¾c£ØSO42-£©£¾c£ØNH4+£© | |
| C£® | de¶ĪÉĻµÄµć¾łĀś×ć¹ŲĻµŹ½£ŗc£ØNH4+£©+c£ØNa+£©£¾2c£ØSO42-£© | |
| D£® | aµćµ½bµćµÄ¹ż³ĢÖŠ£¬ČÜŅŗµÄµ¼µēÄÜĮ¦ŌöĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦ŗóÉś³ÉNOµÄĢå»żĪŖ28 L | B£® | ĖłµĆČÜŅŗÖŠc£ØFe2+£©£ŗc£ØFe3+£©=1£ŗ1 | ||
| C£® | ĖłµĆČÜŅŗÖŠc£ØNO3-£©=2.75 mol/L | D£® | ĖłµĆČÜŅŗÖŠµÄČÜÖŹÖ»ÓŠFeSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōö“ó | B£® | ¼õŠ” | C£® | ²»±ä | D£® | ĪŽ·ØÅŠ¶Ļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Al±ČCu»īĘĆ£¬AlĪŖøŗ¼«£¬Cu¼«ÉĻĪö³öNO2 | |
| B£® | Cu±ČAl»īĘĆ£¬CuĪŖøŗ¼«£¬Al¼«ÉĻĪö³öCu | |
| C£® | CuĪŖøŗ¼«£¬µē¼«·“Ó¦£ŗCu-2e-ØTCu2+ | |
| D£® | AlĪŖÕż¼«£¬µē¼«·“Ó¦£ŗ2H++2e-ØTH2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņ»¶ØĪĀ¶ČĻĀ£¬·“Ó¦MgCl2£Ø1£©ØTMg£Ø1£©+Cl2£Øg£©µÄ”÷H£¼0£¬”÷S£¾0 | |
| B£® | HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=-57.3kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČĪŖ”÷H=2”Į£Ø-57.3£©kJ/mol | |
| C£® | Ķ·Ö±šÓėÅØHNO3”¢Ļ”HNO3·“Ó¦£¬»¹Ō²śĪļ·Ö±šĪŖNO2”¢NO£¬ĖłŅŌÅØHNO3Ńõ»ÆŠŌŠ”ÓŚĻ”HNO3 | |
| D£® | ¶ŌÓŚ·“Ó¦2H2O2ØT2H2O+O2”ü£¬¼ÓČėMnO2»ņÉżøßĪĀ¶Č¶¼ÄܼÓæģO2µÄÉś³ÉĖŁĀŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com