
【题目】孔雀石的主要成分是![]() ,还含有少量
,还含有少量![]() 、
、![]() 等杂质,实验室以孔雀石为原料制备硫酸铜晶体流程如下:
等杂质,实验室以孔雀石为原料制备硫酸铜晶体流程如下:

已知相关氢氧化物沉淀的pH范围如下:
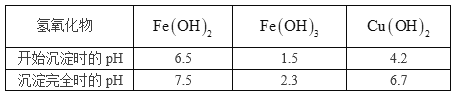
完成下列填空:
(1)滤液1中含有的金属阳离子有_______________。
(2)步骤②中所用的试剂X是________(选填编号)。
a. Fe粉 b. ![]() c. 氨水 d. KSCN
c. 氨水 d. KSCN
(3)步骤③中加入CuO的目的是________________________________________。
(4)由滤液3得到硫酸铜晶体,需要经过的步骤依次有:_________、________、过滤等。
(5)为测定所得晶体中结晶水的![]() 值,可采用加热法。取
值,可采用加热法。取![]() g晶体灼烧至结晶水全部失去,称得无水硫酸铜的质量bg。
g晶体灼烧至结晶水全部失去,称得无水硫酸铜的质量bg。
①晶体应盛装在________(填仪器名称)中进行灼烧。
②确认结晶水已全部失去的方法是___________________________。
③![]() 值的表达式为______________(用
值的表达式为______________(用![]() 、
、![]() 表示)。
表示)。
④实验结果发现测得结晶水数量![]() 偏高,可能的原因有___________(任写一种)。
偏高,可能的原因有___________(任写一种)。
【答案】 Cu2+、Fe2+ b 调节溶液的pH,使Fe3+沉淀的同时不引入新的杂质 蒸发浓缩 降温结晶 坩埚 前后两次称量无水硫酸铜的质量差小于0.001g 80(a-b)/9b 加热前称量时坩埚未完全干燥、加热过程中有少量晶体溅出、加热时坩埚内质量变黑等,合理即可
【解析】试题分析:由流程可知,孔雀石经稀硫酸溶解后,其中的碱式碳酸铜和碳酸亚铁皆可溶解,过滤得到硫酸铜和硫酸亚铁溶液,向滤液中加入氧化剂X把亚铁离子氧化,再加入CuO调节溶液的pH,除去溶液中的铁离子,过滤,将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥即可得到产品。
(1)滤液1中含有的金属阳离子有Cu2+、Fe2+。
(2)步骤②中所用的试剂X是氧化剂,以双氧水为最佳,其他几个不能把亚铁离子氧化,故选b。
(3)步骤③中加入CuO的目的是调节溶液的pH,使Fe3+沉淀的同时不引入新的杂质。
(4)由滤液3得到硫酸铜晶体,需要经过的步骤依次有:蒸发浓缩、降温结晶、过滤等。
(5)为测定所得晶体中结晶水的![]() 值,可采用加热法。取
值,可采用加热法。取![]() g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg。
g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg。
①通常在坩埚中灼烧固体,故晶体应盛装在坩埚中进行灼烧。
②确认结晶水已全部失去的方法是前后两次称量无水硫酸铜的质量差小于0.001g。
③![]() g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg,则结晶水的质量为(a-b)g,结晶水的物质的量为
g晶体的烧至结晶水全部失去,称得无水硫酸铜的质量bg,则结晶水的质量为(a-b)g,结晶水的物质的量为![]() ,bg硫酸铜的物质的量为
,bg硫酸铜的物质的量为![]() ,所以,
,所以, ![]() 值的表达式为80(a-b)/9b。
值的表达式为80(a-b)/9b。
④实验结果发现测得结晶水数量![]() 偏高,可能的原因有:加热前称量时坩埚未完全干燥、加热过程中有少量晶体溅出、加热时坩埚内质量变黑(硫酸铜部分分解生成黑色的氧化铜)等。
偏高,可能的原因有:加热前称量时坩埚未完全干燥、加热过程中有少量晶体溅出、加热时坩埚内质量变黑(硫酸铜部分分解生成黑色的氧化铜)等。


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、P、Q为前四周期元素,且原子序数依次增大。X基态原子的L层有3个单电子,Z是周期表中电负性最大的元素;Y与P为同主族元素,且P基态原子的M层电子数为K层的3倍;Q2+离子的3d轨道上有9个电子。回答下列问题。
(1)基态Y原子的价电子排布图是____;P所在周期中第一电离能最大的主族元素是__________ (元素名称)。
(2)XY3-中,中心原子的杂化方式为____________;XY2-离子的立体构型是_______________。
(3)X 的氢化物比Y的氢化物沸点低的原因是_________________________。
(4)X的氢化物易形成配位键,而XZ3不易形成配位键,原因是_____________________。
(5)Y 与Q所形成的化合物晶体晶胞如图所示,该晶体的化学式:______________;晶胞参数如图所示,则该晶胞密度是_______________g·cm-3。(列式并计算结果,保留小数点后一位)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.K+的结构示意图: ![]()
B.B、基态氮原子的电子排布图 ![]()
C.水的电子式: ![]()
D.D、基态铬原子(24Cr)的价电子排布式:3d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石蜡油分解的实验装置如下图所示。在试管①中加入石蜡油和氧化铝;试管②放在冷水中;试管③中加入酸性高锰酸钾溶液;试管④中加入溴水。

分析回答下列问题:
(1)试管①中加入氧化铝的作用是________________________________________________。
(2)试管②内看到的实验现象是__________________________________________________。
(3)试管③中看到的实验现象为__________________________________________________。
(4)试管④中看到的实验现象为__________________________________________________。
(5)通过本实验说明____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制玻璃时,发生的主要反应的化学方程式为: ![]()
![]()
![]()
完成下列填空:
(1)钠原子核外具有______种不同能量的电子,钠元素在周期表中的位置为____________。
(2)在上述反应中,反应物和生成物的晶体类型共有_____种,写出气体产物的电子式_______________。
(3)上述物质中的非金属元素原子半径由大到小顺序为___________(用元素符号表示),下列能判断它们的非金属性强弱的依据是:________(选填编号)。
a. 气态氢化物的熔沸点 b. 最高价氧化物对应水化物的酸性
c. 气态氢化物的热稳定性 d. 三种元素两两形成的化合物中电子对偏向
(4)常温下,相同物质的量浓度的![]() 和
和![]() 溶液中,
溶液中, ![]() _____
_____ ![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(5)向10mL一定浓度的![]() 溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原
溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原![]() 溶液的物质的量浓度为__________。在滴入盐酸的整个过程中,溶液中
溶液的物质的量浓度为__________。在滴入盐酸的整个过程中,溶液中![]() 的变化情况是______________。
的变化情况是______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.下列说法不正确的是( )

A. 该反应的化学方程式为3X+Y![]() 2Z
2Z
B. 容器内混合气体的平均摩尔质量保持不变表明该反应一定达到平衡状态
C. 平衡时,体系的压强是开始时的1.8倍
D. 平衡时,Y的体积分数为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羚羊角或犀牛角是治疗创伤的中药方剂中用量极少的成分,但是缺少这味药,疗效将大大下降甚至无效。已知动物的角主要由死亡细胞的角化(变性)蛋白质组成,则羚羊角等的有效成分最可能是( )
A. 特殊活性的蛋白质
B. DNA
C. 微量元素
D. 大量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
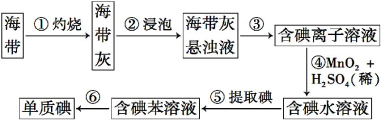
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_________(从下列仪器中选出所需的仪器,用标号字母填写空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘的苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A.用银氨溶液检验某病人是否患糖尿病
B.酶不属于蛋白质
C.在植物油中滴入溴水,溴水褪色
D.在鸡蛋白溶液中滴入浓HNO3,微热会产生黄色物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com