
【题目】某同学帮助水质监测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用。
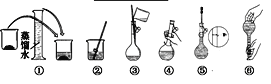

(1)该同学应选择____mL的容量瓶。
(2)其操作步骤如图所示,则上图框中操作应在图中__________ (填选项字母)之间。
A.②与③ B.①与② C.③与④
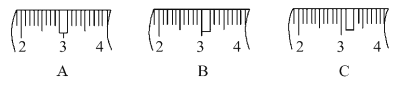
(3)该同学应称取NaOH固体____g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小____(填字母),并在下图中选出能正确表示游码位置的选项____(填字母)。
附表 砝码规格
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
(4)下列操作对所配溶液的浓度大小有何影响(填“偏大” “偏小”或“无影响”)。
①定容时,俯视读数,浓度会________;②转移溶液过程中,少量液体溅出来,浓度会____________;
③容量瓶未干燥,浓度会__________;
④定容摇匀后发现溶液凹面低于刻度线,浓度会______________。
【答案】 500 c 10.0 cd c 偏大 偏小 无影响 无影响
【解析】(1)选取容量瓶的规格应该等于或稍大于配制溶液的体积,实验室没有480mL容量瓶,所以应该选500mL容量瓶;
(2)如图所示的操作为移液洗涤后向容量瓶内加水,应在转移与定容之间,即应在④到⑤之间,故答案为c;
(3)配制500mL0.5molL-1NaOH溶液需要氢氧化钠的质量为0.5L×0.5mol/L×40g/mol=10.0g;氢氧化钠具有腐蚀性且易潮解,应放在烧杯内称量,根据氢氧化钠与烧杯总质量为10.0g+23.1g=33.1g,故应选择20g与10g的砝码,即选择cd;由表中升高可知,最小的砝码为5g,故游码的最大刻度为5g,故小于5g所以游码,所以游码应在3.1g的位置,故选择C;
(4))①定容时,俯视读数,溶液体积偏小,配制溶液浓度偏大;
②转移溶液过程中,少量液体溅出来,溶质的物质的量偏小,浓度会偏小;
③容量瓶使用时未干燥,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度无影响;
④定容摇匀后发现溶液凹面低于刻度线,部分溶液附着在瓶壁上,浓度无影响。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】对于反应2X(g) +Y(g)![]() 2Z(g),下列说法中正确的是
2Z(g),下列说法中正确的是
A. 由于K=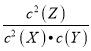 ,随着反应的进行,Z的浓度不断增大,X、Y浓度不断减小,平衡常数不断增大
,随着反应的进行,Z的浓度不断增大,X、Y浓度不断减小,平衡常数不断增大
B. 当温度不变时,增大反应物的浓度,使K变小
C. 可逆反应达到平衡时,逆反应便立即停止了
D. 温度发生变化,上述反应的K值也发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】走进化学变化的微观世界,有利于进一步认识化学变化,如图是某化学变化的微观示意图,A、B、C分别表示不同类别的原子,据图回答问题: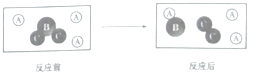
(1)该化学反应中生成物的分子个数比为;
(2)该化学反应的基本类型为 .
(3)由 ![]() 微粒构成的物质属于(填“单质”或“化合物”).
微粒构成的物质属于(填“单质”或“化合物”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸生产中炉气转化反应为2SO2(g)+O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数 (SO3%)随温度(T)的变化如曲线I所示。下列判断不正确的是
2SO3(g)。研究发现,SO3的体积分数 (SO3%)随温度(T)的变化如曲线I所示。下列判断不正确的是
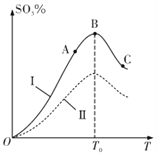
A. 该反应的正反应为放热反应
B. 曲线I上A、C两点反应速率的关系是:VA<VC
C. 反应达到B点时,2V正(O2) = V逆(SO3)
D. 已知V2O5的催化效果比Fe2O3好,若I表示用V2O5作催化剂的曲线,则Ⅱ可表示用Fe2O3作催化剂的曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是
①C(s) + H2O(g)==CO(g)+H2(g) ΔH1=a kJmol-1
②CO(g) + H2O(g)==CO2(g)+H2(g) ΔH2=b kJmol-1
③CO2(g)+3H2(g)==CH3OH(g)+H2O(g) ΔH3 =c kJmol-1
④2CH3OH(g) ==CH3OCH3(g)+H2O(g) ΔH4=d kJmol-1
A. 反应①②为反应③提供原料气
B. 反应③也是CO2资源化利用的方法之一
C. 反应CH3OH(g)== ![]() CH3OCH3(g)+
CH3OCH3(g)+ ![]() H2O(1)的ΔH =
H2O(1)的ΔH =![]() kJmol-1
kJmol-1
D. 反应 2CO(g)+4H2(g) ==CH3OCH3(g)+H2O(g)的ΔH= (2b+2c+d) kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某元素的原子核外电子排布中,K电子层和L电子层的电子数之和等于M电子层和N电子层的电子数之和。则该元素的核电荷数为
A. 12 B. 17 C. 20 D. 30
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学探究小组欲制取少量氢氧化钠溶液.他们把饱和石灰水加入盛有碳酸钠溶液的烧杯中,经充分搅拌、过滤,得到样品溶液.
(1)写出反应的化学方程式:;
(2)小组同学对得到的样品溶液是否为纯净的氢氧化钠溶液产生怀疑,决定对其溶质成份进行探究.【提出猜想】
猜想一:只含氢氧化钠
猜想二:含有氢氧化钠、氢氧化钙
猜想三:含有氢氧化钠、碳酸钠
【实验探究】小组同学发现,只要用反应物(饱和石灰水和碳酸铵溶液)就可以验证猜想.他们取少量样品溶液进行下列实验:
实验操作 | 实现现象 | 实验结论 |
① | 猜想二不正确 | |
② | 猜想三正确 |
(3)【交流讨论】甲同学认为要验证猜想二不正确,也可往样品溶液中通入;受该同学的启发,小组同学认为要验证猜想三正确,也可以在样品溶液中滴加盐酸.
(4)【实验评价】乙同学往样品溶液中滴入盐酸,刚开始没有观察到明显现象,试分析原因 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com