
| 实验 | 现象 | 结论 | |
| A | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | 非金属性:Cl>C>S |
| B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO32-中的一种或几种 |
| C | 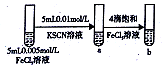 | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
| D | 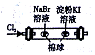 | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.HCl不是最高价含氧酸,无法判断三者非金属性强弱;
B.原溶液中还可能含有银离子;
C.增大铁离子浓度,有利于生成络离子;
D.氯气可氧化溴离子、碘离子.
解答 解:A.用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中,能够说明酸性HCl>H2SiO3>H2CiO3,由于HCl不是含氧酸,无法比较Cl与Si的非金属性强弱,故A错误;
B.向某溶液先滴加硝酸酸化,再滴加BaCl2溶液,生成的白色沉淀可能为AgCl,原溶液中可能含有银离子,不一定含有SO42-、SO32-、HSO32-,故B错误;
C.增大铁离子浓度,有利于生成络离子,试管b比试管a中溶液的红色深,平衡向正反应方向移动,故C正确;
D.氯气可氧化溴离子、碘离子,则该实验不能得到Br2>I2,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、反应原理等为解答的关键,涉及非金属性比较、离子检验、平衡移动、氧化性比较等,注意实验评价性分析,题目难度不大.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
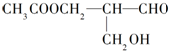 在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性,下面的物质有光学活性:发生下列反应后生成的有机物无光学活性的是( )| A. | 与甲酸发生酯化反应 | B. | 与新制的氢氧化铜作用 | ||
| C. | 与银氨溶液作用 | D. | 在催化剂存在下与H2作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ksp(AB2)<Ksp(CD),说明AB2的溶解度小于CD的溶解度 | |
| B. | 在ZnS的沉淀溶解平衡体系中加入蒸馏水,ZnS的Ksp不变 | |
| C. | 已知Ksp(AgCl)>Ksp(AgI),则反应AgCl(s)+I-(aq)=AgI(s)+Cl-(aq)能够发生 | |
| D. | 在CaCO3的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 58 | B. | 173 | C. | 3 | D. | 128 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
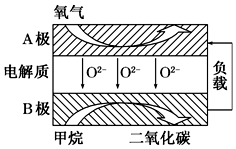 以甲烷为燃料的新型电池得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图.下列说法错误的是( )
以甲烷为燃料的新型电池得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图.下列说法错误的是( )| A. | 以甲烷为燃料,其成本大大低于以氢气为燃料的传统燃料电池 | |
| B. | A电极为电池正极,发生还原反应 | |
| C. | B电极反应式为CH4+4O2--8e-═CO2+2H2O | |
| D. | 若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol•L-1的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为22.4L(标准状况下) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KI被氧化成KOH | |
| B. | KI是离子化合物,I2是共价化合物 | |
| C. | 1 mol O3 在反应中得到4 mol 电子 | |
| D. | KOH中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在T°C时,某溶液中c(H+)=$\sqrt{{K}_{W}}$,则该溶液一定显中性 | |
| B. | 25°C时,如弱酸与强碱溶液的pH之和等于14,则它们等体积混合液呈酸性 | |
| C. | 常温下,pH相等的NaOH溶液与氨水稀释后保持pH仍然相等,则氨水加水多 | |
| D. | 体积和pH均相等的HCl与CH3COOH溶液分别与足量锌粒反应,放出H2一样多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com