
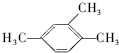
 1,3,4-三甲苯
1,3,4-三甲苯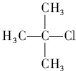 2-甲基-2-氯丙烷
2-甲基-2-氯丙烷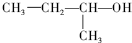 2-甲基-1-丙醇
2-甲基-1-丙醇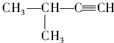 3-甲基-1-丁炔
3-甲基-1-丁炔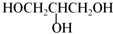
分析 (1)根据碳元素守恒,碳元素质量分数越大,燃烧生成二氧化碳的量越大;
(2)A、 的名称为:1,2,4-三甲苯;
的名称为:1,2,4-三甲苯;
B、 的名称为:2-甲基-2-氯丙烷;
的名称为:2-甲基-2-氯丙烷;
C、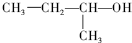 的名称为:1-甲基-1-丙醇;
的名称为:1-甲基-1-丙醇;
D、 的名称为:3-甲基-1-丁炔;
的名称为:3-甲基-1-丁炔;
(3)能与水分子形成氢键的物质在水中的溶解度较大,形成氢键数目越多,溶解度越大,据此分析;
(4)A.乙醛发生银镜反应,体现乙醛的还原性;
B.甲醛与新制的氢氧化铜悬浊液反应,体现甲醛的还原性;
C.丙酮与氢气发生加成,有机加氢发生还原反应,本身是氧化剂;
D.乙烯使酸性KMnO4溶液褪色,乙烯是还原剂;
E.乙烯使溴水褪色,发生加成反应;
F.乙醇在铜的催化下与氧气作用生成乙醛,体现乙醇的还原性.
解答 解:(1)碳元素质量分数越大,燃烧生成二氧化碳的量越大,分子式依次为:①甲醇②乙醇③乙二醇④丙三醇⑤乙烯,碳元素质量分数为:乙烯>乙醇>丙三醇>乙二醇>甲醇,故相同质量完全燃烧,生成二氧化碳的量:⑤>②>④>③>①,
故答案为:⑤>②>④>③>①;
(2)A、 的名称为:1,2,4-三甲苯,故错误;
的名称为:1,2,4-三甲苯,故错误;
B、 的名称为:2-甲基-2-氯丙烷,故正确;
的名称为:2-甲基-2-氯丙烷,故正确;
C、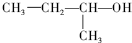 的名称为:1-甲基-1-丙醇,故错误;
的名称为:1-甲基-1-丙醇,故错误;
D、 的名称为:3-甲基-1-丁炔,故正确;
的名称为:3-甲基-1-丁炔,故正确;
故选:A.C;
(3)①HOCH2CH2CH2OH ②CH3CH2CH2OH
③CH3CH2COOCH3 ④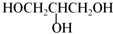
这些物质中CH3CH2COOCH3 不能与水形成氢键,则溶解度最小,分子中含有羟基数目越多,与水形成的氢键越多,则溶解度越大,所以溶解度:HOCH2CH(OH)CH2OH>HOCH2CH2CH2OH>CH3CH2CH2OH>CH3CH2COOCH3,即④>①>②>③,故答案为:④>①>②>③;
(4)A.乙醛发生银镜反应,体现乙醛的还原性,故正确;
B.甲醛与新制的氢氧化铜悬浊液反应,体现甲醛的还原性,故正确;
C.丙酮与氢气发生加成,有机加氢发生还原反应,本身是氧化剂,故错误;
D.乙烯使酸性KMnO4溶液褪色,乙烯是还原剂,故正确;
E.乙烯使溴水褪色,发生加成反应,故错误;
F.乙醇在铜的催化下与氧气作用生成乙醛,体现乙醇的还原性,故正确,
故选:A.B.D.F.
点评 本题考查了有机物的溶解性,根据氢键对物质溶解性的影响分析解答即可,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | Y极是正极 | B. | X极发生氧化反应 | ||
| C. | 电子由X极经外电路流向Y极 | D. | 此电池的电解质溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
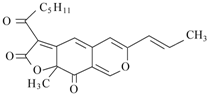 红曲色素是通过中国传统工业发酵得到的天然色素,用作食品色素安全性很高,同时具有抑菌、防腐和保健作用.其中一种成分--红斑红素结构如图所示,下列有关红斑红素的说法正确的是( )
红曲色素是通过中国传统工业发酵得到的天然色素,用作食品色素安全性很高,同时具有抑菌、防腐和保健作用.其中一种成分--红斑红素结构如图所示,下列有关红斑红素的说法正确的是( )| A. | 分子中环上的所有原子都在同一平面上 | |
| B. | 红斑红素的分子式为C21H24O5 | |
| C. | 1 mol该物质能与5 mol Br2发生加成反应 | |
| D. | 1 mol 该物质水解时能消耗2 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
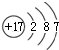 ②CCl4的结构式:
②CCl4的结构式: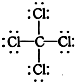
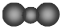 ④Na2S的电子式:
④Na2S的电子式:
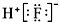 ⑦I-131:7853I
⑦I-131:7853I ⑨乙烯的结构简式:CH2CH2.
⑨乙烯的结构简式:CH2CH2.| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=4b+3c | B. | a=4b+c | C. | a:b=4:1 | D. | a:b=4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
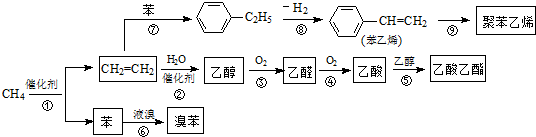
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>M | |
| B. | 1molW溶于足量水中完全反应其转移2mol电子 | |
| C. | YZ2溶于水形成的溶液具有较强的氧化性 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定只有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com