
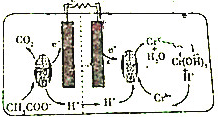
 如图所示的微生物燃料电池在净化废水的同时能回收能源或得到有价值的化学品,下列有关说法正确的是( )
如图所示的微生物燃料电池在净化废水的同时能回收能源或得到有价值的化学品,下列有关说法正确的是( )| A. | 该电池能够在高温下工作 | |
| B. | 得到的有价值的化学品为CO2和Cr(OH)3 | |
| C. | 右室中的电极为负极 | |
| D. | 1molCH3COO-转化为CO2得到4mol电子 |
分析 由电解池装置图可知H+向右移动,则右室电极为正极,发生还原反应,H+得电子生成氢气,同时在正极室生成Cr(OH)3,左室发生氧化反应,CH3COO-被氧化生成CO2,为原电池的负极,以此解答该题.
解答 解:由电解池装置图可知H+向右移动,则右室电极为正极,发生还原反应,H+得电子生成氢气,同时在正极室生成Cr(OH)3,左室发生氧化反应,CH3COO-被氧化生成CO2,为原电池的负极,
A.温度较高时,可使蛋白质变性,该微生物电池不能在高温下工作,故A错误;
B.由以上分析可知负极发生氧化反应生成CO2,正极生成Cr(OH)3,故B正确;
C.由分析可知右室中的电极为正极,故C错误;
D.CH3COO-中C平均元素化合价为0,1molCH3COO-转化为CO2得到8mol电子,故D错误.
故选B.
点评 本题考查原电池知识,为高频考点,侧重学生的分析能力的考查,答题时注意把握题给信息,结合氢离子的定向移动判断原电池的正负极,易错点为D,注意有机物中C元素化合价的判断,难度中等.


科目:高中化学 来源: 题型:填空题
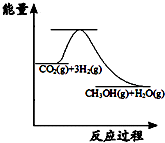 目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);图表示该反应进行过程中能量的变化.(单位为:kJ•mol-1)该反应是放热(填“吸热”或“放热”)反应.△H<0(填“>”或“<”).
目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);图表示该反应进行过程中能量的变化.(单位为:kJ•mol-1)该反应是放热(填“吸热”或“放热”)反应.△H<0(填“>”或“<”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表是元素周期律的具体表现形式 | |
| B. | 元素的性质随原子序数递增而呈现周期性变化的根本原因是随原子序数的递增原子的核外电子排布呈现周期性变化 | |
| C. | 同周期第IA族与第VA族原子序数之差可能是4、14、28 | |
| D. | 同主族原子序数之差不可能是:10、16、18、26、34、36、50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
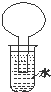 如图所示的装置是某次实验最初的情况(夹持装置省略),烧瓶内盛有等体积的CH4和Cl2,用光照射烧瓶一段时间,下列说法正确的是( )
如图所示的装置是某次实验最初的情况(夹持装置省略),烧瓶内盛有等体积的CH4和Cl2,用光照射烧瓶一段时间,下列说法正确的是( )| A. | 只能生成CH3Cl一种有机物 | B. | 烧瓶内液面不可能上升 | ||
| C. | 大试管内的液体可能会分层 | D. | 向水中加入石蕊试液后无变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
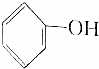 >HCO3-,下列化学方程式不正确的是( )
>HCO3-,下列化学方程式不正确的是( )| A. | 2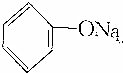 +H2O+CO2→2 +H2O+CO2→2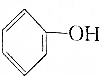 +Na2CO3 +Na2CO3 | B. | 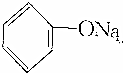 +H2O+CO2→ +H2O+CO2→ +NaHCO3 +NaHCO3 | ||
| C. |  +Na2CO3→ +Na2CO3→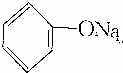 +NaHCO3 +NaHCO3 | D. | 2 +2Na→2 +2Na→2 +H2↑ +H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
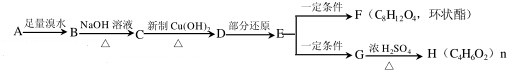
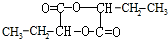 ,H
,H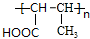 .
.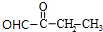 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$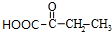 +Cu2O+2H2O,E→F2
+Cu2O+2H2O,E→F2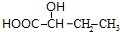 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
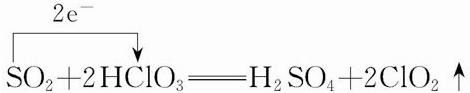 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ②③④⑤⑥⑦ | C. | ②③④⑤⑦ | D. | 只有③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是分子组成相差一个或若干个CH2原子团的物质,彼此一定是同系物 | |
| B. | 分子式为C5H12O且氧化产物能发生银镜反应的醇有6种 | |
| C. | 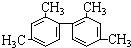 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 | |
| D. | 1mol β-紫罗兰酮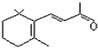 与1mol H2发生加成反应可得到3种不同产物 与1mol H2发生加成反应可得到3种不同产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com