
【题目】选择萃取剂将碘水中的碘萃取出来,这种萃取剂应具备的性质是( )B
A.不溶于水,且必须易与碘发生化学反应 B.不溶于水,且必须比水密度小
C.不溶于水,且必须比水密度大 D.不溶于水,且比水更容易使碘溶解
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 一定条件下可以用H2除去乙烷中混有的乙烯
B. 苯和四氯化碳都能萃取溴水中的溴
C. 乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法分离
D. 甲烷、乙烯和苯在工业上都可通过石油分馏得到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生活中用途比较广泛。
(1)高铁酸钠(Na2FeO4)是一种新型的绿色消毒剂和高容量电池材料。将Fe(NO3)3与NaClO混合后,在碱性条件下发生反应可制得高铁酸钠,该反应的离子方程式为________________________。
(2)四氧化三铁(Fe3O4)常用作颜料、磁流体材料、催化剂和电子材料等。共沉淀法是目前制备纳米Fe3O4的重要方法之一,其流程如图所示:

①为得到较纯净的纳米Fe3O4,FeSO4·7H2O与FeCl3·6H2O的物质的量之比最好为________。但实际操作时,却很难控制这一比例,原因是_____________________________。
②在最佳投料比条件下,检验Fe3O4是否沉淀完全的实验操作是_________________________。
(3)绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。测定绿矾产品中FeSO4·7H2O含量的方法如下:
a.称取3.0 g绿矾产品,配制成250.00 mL溶液;
b.量取25.00 mL a中溶液于锥形瓶中;
c.用0.010 00 mol·L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液的平均体积为20.00 mL。滴定时发生反应的离子方程式为5Fe2++MnO![]() +8H+===5Fe3++Mn2++4H2O。
+8H+===5Fe3++Mn2++4H2O。
①0.010 00 mol·L-1KMnO4溶液应置于如图所示仪器________(填“甲”或“乙”)中,滴定终点的现象是__________________________________。
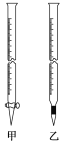
②产品中FeSO4·7H2O的质量分数为________(小数点后保留1位数字)。
③若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),可能的原因有___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是( )
A. 表示硫的燃烧热的热化学方程式S(s)+![]() O2(g)=SO3(g);ΔH=-315 kJ·mol-1
O2(g)=SO3(g);ΔH=-315 kJ·mol-1
B. 表示中和热的热化学方程式NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);ΔH=-57.3 kJ·mol-1
C. 表示H2燃烧热的热化学方程式H2(g)+![]() O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g);ΔH=-241.8 kJ·mol-1
D. 表示CO燃烧热的热化学方程式2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2剧毒,致死量为0.3g,万一不慎误服,应大量吞服鸡蛋清及适量解毒剂,此解毒剂应是
A. AgNO3 B. CuSO4 C. Na2CO3 D. MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铝合金投入一定浓度的100 mL盐酸中,使合金全部溶解,向所得溶液中滴加5.00 mol/L的NaOH溶液至过量,生成沉淀的质量与加入NaOH溶液的体积的关系如图所示。
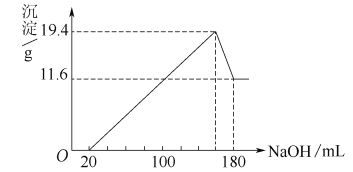
试求:(1)原合金中铝的质量分数。
(2)盐酸的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( )
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中
③Al(OH)3、Cu(OH)2受热易分解,Fe(OH)3受热也易分解
④不能用电解熔融 的AlCl3来制取金属铝;也不能用电解熔融的MgCl2来制取金属镁
A.①④ B.②④
C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用如图装置制取溴苯并证明苯和液溴发生的是取代反应。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
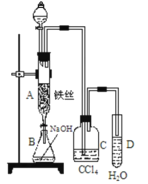
(1)写出 A 中发生反应的化学方程式_____________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是__________,写出有关反应的离子方程式____________。
(3)C中盛放 CCl4的作用是___________________。
(4)为证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液, 若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入___________,现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合氯化铝晶体是介于 AlCl3和 Al(OH)3之间的一种水溶性无机高分子聚合物, 是一种高效无机水处理剂, 其制备原料主要是铝加工行业的废渣--铝灰,它主要含 Al2O3、 Al,还有一些不溶于酸的杂质.聚合氯化铝生产工艺流程如下:

(1)反应中副产品E是_________(用化学式表示);
(2)生产过程中可循环使用的物质是_________(用化学式表示);
(3)为使得到的晶体较纯净,生产过程中使pH升高的c 物质可选用_________(填编号);
a. NaOH b. Al c.氨水 d. A12O3 e. NaAlO2
(4)聚合氯化铝晶体的化学式可表示为: [A12(OH)nCl6-n·xH2O]m,实验室为测定化学式中n的值,进行如下实验:
①称取 ag晶体,制成粉末,加热至质量不再变化时,得到bg氧化铝固体.此过程可能用到的下列仪器有___________;(填编号)
a.蒸发皿 b.坩埚 c.研钵 d.试管
②另取ag晶体,进行如下操作:用A 酸溶解→加足量AgNO3溶液→操作c →烘干→称量为c g 固体.试剂A为_______,操作C为_________(填操作名称).n=_________(用含a、b、c的代数式表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com