
 ��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棬п�����ԭ������Ϊ65����
��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棬п�����ԭ������Ϊ65����| n(H2) |
| n(SO2) |
| 64CV-2m |
| m |
| 64CV-2m |
| m |
| n(H2) |
| n(SO2) |
| 1.30g |
| 65g/mol |
| m |
| 32 |
| m |
| 64 |
| m |
| 32 |
| m |
| 32 |
| m |
| 32 |
| n(H2) |
| n(SO2) |
(CV-
| ||
|
| 64CV-2m |
| m |
| 64CV-2m |
| m |


 ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д� �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
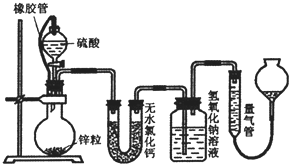 ��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪS02��Ҳ�ɱ���ԭΪ������ijУ�о���ѧϰС�������ʵ����֤��һ��ʵ�����������ݲⶨ����ؼ��㣮
��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪS02��Ҳ�ɱ���ԭΪ������ijУ�о���ѧϰС�������ʵ����֤��һ��ʵ�����������ݲⶨ����ؼ��㣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
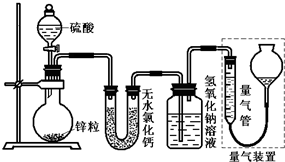 ��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10l kPa���¶�Ϊ0�棩��
��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10l kPa���¶�Ϊ0�棩���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棩��
��1��������ƿ�з���1.30gп������c mol��L H2SO4��Ӧ��Ϊ��֤ʵ����۵Ŀɿ��������ܵ����˹����_____________ ��
A��200mL B��400 mL C��500mL
��2����1.30gп����ȫ�ܽ⣬��������ϴ��ƿ����l.28g ����Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ��___________________________________��
��3������ƿ��Ͷ��a gп����ȫ��Ӧ����������ϴ��ƿ����b g������ƿ���ռ���Vm�����壬���У�ag��65g��mol��1��bg��64g��mol��1��V mL / 22400 mL��mol��1�����ݵ�ԭ����____________________________��
��4��������ƿ��Ͷ��d gп������һ������cmol��L Ũ����V L����ַ�Ӧ��п��ʣ�࣬�����������ϴ��ƿ����mg��������ʵ����̲����������У�n��H2��/n��SO2����_______________���ú���ĸ�Ĵ���ʽ��ʾ����������ʢ����ˮ�Ȼ��Ƶ�U�ܣ�n��H2��/n��SO2������ֵ�� ����ƫ��ƫС����Ӱ�죩
��5�� ��Ӧ������Ϊ��ȷ�ز�������������������ڶ���ʱӦע�⣺
��
��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�Ƹ���ѧ2011������꼶ʮ���¿���ѧ���� ���ͣ������
��15�֣���ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棩��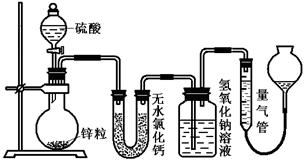
��1��������ƿ�з���1.30gп������c mol��L H2SO4��Ӧ��Ϊ��֤ʵ����۵Ŀɿ��������ܵ����˹����_____________ ��
A��200 mL B��400 mL C��500mL
��2����1.30gп����ȫ�ܽ⣬��������ϴ��ƿ����l.28g ����Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ��_______________________________________��
��3������ƿ��Ͷ��a gп����ȫ��Ӧ����������ϴ��ƿ����b g������ƿ���ռ���Vm�����壬���У�ag��65g��mol��1��bg��64g��mol��1��V mL / 22400 mL��mol��1�����ݵ�ԭ����____________________________��
��4��������ƿ��Ͷ��d gп������һ������c mol��L Ũ����V L����ַ� Ӧ��п��ʣ�࣬�����������ϴ��ƿ����mg��������ʵ����̲����������У�n��H2��/n��SO2����_______________���ú���ĸ�Ĵ���ʽ��ʾ����������ʢ����ˮ�Ȼ��Ƶ�U�ܣ�n��H2��/n��SO2������ֵ��
Ӧ��п��ʣ�࣬�����������ϴ��ƿ����mg��������ʵ����̲����������У�n��H2��/n��SO2����_______________���ú���ĸ�Ĵ���ʽ��ʾ����������ʢ����ˮ�Ȼ��Ƶ�U�ܣ�n��H2��/n��SO2������ֵ��
����ƫ��ƫС����Ӱ�죩
��5�� ��Ӧ������Ϊ��ȷ�ز�������������������ڶ���ʱӦע�⣺
�� ��
�� ��
�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com