
【题目】人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒, 因为亚硝酸盐会使Fe2+离子转变成Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有
A.酸性 B.碱性 C.氧化性 D.还原性
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】【2015浙江理综化学】Ⅰ.请回答:
(1)H2O2的电子式___________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_____________。
(4)完成以下氧化还原反应的离子方程式:
( )MnO4-+( )C2O42-+______=( )Mn2++( )CO2↑+________
Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl3反应得到NaAlH4的化学方程式__________。
(3)NaAlH4与水发生氧化还原反应的化学方程式__________。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 。
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。
判断该同学设想的制备和验纯方法的合理性并说明理由___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组设计了如下图装置,不断改变A中溶液成份反应以探究SO2气体的性质
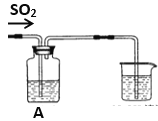
(1)如果A中盛有氢硫酸溶液,通入SO2气体后可观察到有浅黄色浑浊出现,则证明SO2有_________性;写出化学反应方程式____________________________________
(2)如果A中盛有酸性高锰酸钾溶液,通入SO2气体后实验现象是________________,证明SO2有_______性。
(3)如果A中盛有稀硝酸钡溶液, 通入SO2气体后可观察到出现白色沉淀,有无色NO气体生成,写出离子反应方程式_______________________________________________。
(4)如果A中盛有氯化钡溶液,通入SO2气体后本应无沉淀生成,但同学们发现在溶液中也有少量白色沉淀。甲同学把此白色沉淀过滤出来,该沉淀不溶于盐酸。该同学猜测是由于装置中空气没有排净,参与了反应,试写出离子反应方程式_____________________________________。
(5)如果A中盛有纯碱水溶液,写出向A中缓缓加入少量SO2的离子反应方程式____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列3种有机化合物A:CH2=CH2、 B:、 C:CH3COOH
(1)写出化合物A、C中官能团的名称 、______________;
(2)3种化合物中能使溴的四氯化碳溶液褪色的是 (写名称),该反应的化学方程式为: ,该物质在农业上用作水果的 ;
(3)B的名称是 ,它的分子具有 (填分子构型)结构,是否存在单双键交替结构 (填“是”或“否”);
(4)3种化合物中能与乙醇发生酯化反应的是 (写名称)。该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L固定容积的密闭容器中,在不同反应时间各物质的物质的量的变化情况如图所示。
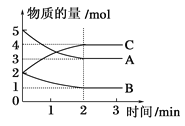
(1)该反应的化学方程式是__________________;
(2)0~2 min,C的平均反应速率为___________;
(3)2 min后,A、B、C各物质的量不再随时间的变化而变化,说明在此条件下,反应已达到了___________状态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施对增大反应速率明显有效的是( )
A. Na与无水乙醇反应时增大无水乙醇的用量
B. Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸
C. 在K2SO4与BaCl2两溶液反应时,增大压强
D. 将炭块磨成炭粉用于燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向饱和氯水中逐滴滴入0.1mol·L-1的氢氧化钠溶液,pH变化如下图所示,列有关叙述正确的是( )
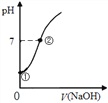
A. ①点所示溶液中只存在HClO的电离平衡
B. ①到②水的电离程度逐渐减小
C. I-能在②点所示溶液中存在
D. ②点所示溶液中:c(Na+)=c(Cl-) + c(ClO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是
A.SO3+H2O===H2SO4
B.2Na2O2+2H2O===4NaOH+O2↑
C.2F2+2H2O===4HF+O2
D.2Na+2H2O===2NaOH+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com