
【题目】由氧化铜、氧化铁、氧化锌组成的混合物ag,加入2mol/L硫酸50mL时固体恰好完全溶解,若将ag该混合物在足量的一氧化碳中加热充分反应,冷却后剩余固体的质量为
A.1.6gB.(a-1.6)gC.(a-3.2)gD.无法确定
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】银精矿主要含有 Ag2S(杂质是铜、锌、锡和铅的硫化物),工业上利用银精矿制取贵金属银,流程图如下图所示。已知“ 氯化焙烧” 能把硫化物转化为氯化物,请回答下列问题:
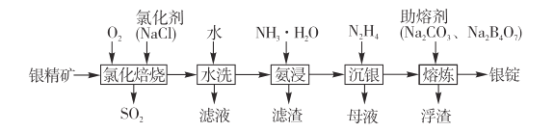
(1)“ 氯化焙烧” 的温度控制在 650~670℃,如果温度过高则对焙烧不利,产率会降低,原因是 ______。
(2)水洗后的滤液中溶质有盐酸盐和大量钠盐,取少量滤液加入盐酸酸化,再滴入氯化钡溶液有白色沉淀生成,此钠盐为_____(填化学式)。
(3)氨浸时发生的化学反应方程式为________。
(4)“ 沉银” 是用 N2H4还原银的化合物。
①N2H4的电子式是_______。
②理论上,1molN2H4完全反应所得到的固体质量是______g。
③向所得母液中加入烧碱,得到的两种物质可分别返回________ 、______工序中循环使用。
(5)助熔剂 Na2CO3和 Na2B4O7有两个作用:一是降低了银的熔点,减少能耗;二是____。利用________的方法可以进一步直接精炼银锭。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应在日常生活中有着广泛的应用,下列有关化学用语和相关说法均正确的是
选项 | 化学反应方程式 | 相关说法 |
A |
| 氧气是氧化产物,氯酸钾既是氧化剂又是还原剂 |
B | Cl2+2Br-=2Cl-+Br2 Zn+Cu2+=Zn2++Cu | 均为单质被还原的置换反应 |
C | 4CuO | 该反应中每生成1molO2,则转移2NA个电子 |
D | 2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑ | 氧化性:Na2O2>Na2FeO4>FeSO4 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A.在火柴头浸取的水溶液中滴入AgNO3溶液,稀硝酸溶液检验氯元素时离子反应:Ag++Cl-=AgCl↓
B.NaNO2溶液中滴加适量稀盐酸:2![]() +2H+=H2O+NO↑+NO2↑
+2H+=H2O+NO↑+NO2↑
C.向Cu(NO3)2溶液中加入过量氨水:Cu2++2NH3H2O= Cu(OH)2↓+2![]()
D.苯酚与三氯化铁溶液反应,得到溶液显紫色:6C6H5O-+Fe3+=[Fe(OC6H5)6]3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pc类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3mol/L,则该溶液溶质的pc=3。下列说法正确的是
A.25°C时,0.01mol/LNa2S水溶液中,pc(H+)+pc(OH-)=14
B.用0.01mol/L的NaOH溶液滴定某浓度的盐酸,滴定过程中pc(OH-)逐渐增大
C.某温度下,弱酸HB的Ka=1×10-5mol/L,则该溶液中pc(H+)+pc(B-)=l0
D.向0.0lmol/L的Ca(HCO3)2溶液中逐渐滴加烧碱溶液,滴加过程中pc(Ca2+)逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,中国科学院大连化物所CO2催化转化为CO的研究获得新成果。下图是使用不同催化剂(NiPc和CoPc)时转化过程中的能量变化,下列说法正确的是
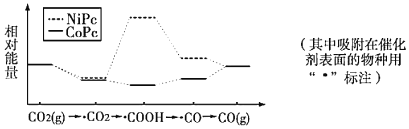
A.CO2(g)→CO(g)+l/2O2(g)过程中能量降低
B.CO2经氧化反应得到COOH
C.该条件下,催化剂NiPc比CoPc对CO2(g)→CO(g)转化效率更高
D.该研究成果将有利于缓解温室效应并解决能源转化问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的回收与利用是科学家研究的热点课题,可利用CH4与CO2制备“合成气”(CO、H2),还可制备甲醇、二甲醚、低碳烯烃等燃料产品。
I.制合成气
科学家提出制备:“合成气”反应历程分两步:
反应①: CH4(g)C(ads)+2H2(g) (慢反应)
反应②:C(ads)+CO2(g)2CO(g) (快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如下图:
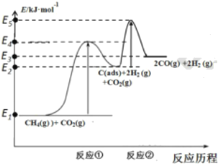
(1) CH4与CO2制备“合成气”的热化学方程式为____。 能量变化图中:E5+E1_______E4+ E2(填“>” 、 “< ” 或 “= ”)。
II.甲醇合成
在某 CO 催化加氢制甲醇的反应体系中,发生的主要反应有:
i. CO2(g) + 3 H2(g)CH3OH(g)+H2O(g)△H1< 0
ii.CO2(g) + H2(g)CO (g)+H2O(g) △H2>0
iii . CO(g)+2H2( g)CH3OH(g) (g) △H3< 0
(2)5MPa 时,往某密闭容器中按投料比n(H2) :n ( CO2) =3:1 充入H2和CO2。反应达到平衡时, 测得各组分的物质的量分数随温度变化的曲线如图所示。
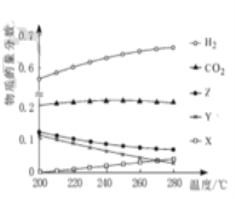
①体系中CO2的物质的量分数受温度的影响不大, 原因是_____。
②250°C时,反应 i i 的平衡常数____1(填“> ”“< ”或“=”)
③下列措施中,无法提高甲醇产率的是____(填标号)。
A.加入适量CO B.增大压强 C.循环利用原料气 D.升高温度
④在下图中画出n(H2)/ n(CO2)随温度变化趋势图_____。
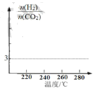
(3)反应i可能的反应历程如下图所示。
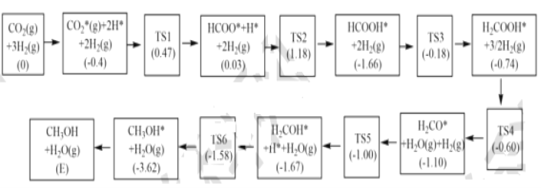
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV)。其中TS表示过渡态、*表示吸附在催化剂上的微粒,反应历程中,生成甲醇的决速步骤的反应方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl![]() NaCl+N2↑+2H2O;关于该反应的下列说法不正确的是( )
NaCl+N2↑+2H2O;关于该反应的下列说法不正确的是( )
A. Na2NO2是氧化剂,NH4Cl是原剂
B. N2既是氧化产物,又是还原产物
C. NH4Cl中氮元素被还原
D. 每生成1molN2转移电子的物质的量为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中A12O3的含量。查阅资料得知,铝土矿的主要成分是A12O3 ,杂质是Fe2O3、SiO2等。从铝土矿中提取A12O3的过程如下:
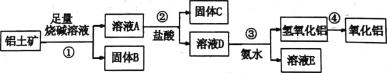
(1)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:______。
(2)第②步用到的分离方法是_______。
(3)请从下面仪器中选出第④步操作不需要的仪器_____________(填字母)
A.蒸发皿 B.玻璃棒 C.泥三角 E.酒精灯 F.坩埚
(4)将实验过程中所得固体准确称量。课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中A12O3 的质量分数__________(结果保留一位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com