
【题目】NA为阿伏加德罗常数的值,下列叙述正确的是
A. 0.5mol熔融的NaHSO4中含有的离子数目为NA
B. 12g金刚石中含有C-C键数目为4NA
C. 25℃时,Ksp(BaSO4)=1×10-10,则饱和BaSO4溶液中Ba2+数目为1×10-5NA
D. 1mol的Na2O和BaO2混合物中含有的阴、阳离子总数为3NA
【答案】A
【解析】A项,熔融的NaHSO4中的离子为Na+、HSO4-,0.5mol熔融的NaHSO4中含有的离子数为NA,正确;B项,n(C)=![]() =1mol,1mol金刚石中含有C—C键数目为2NA,错误;C项,饱和BaSO4溶液中c(Ba2+)=
=1mol,1mol金刚石中含有C—C键数目为2NA,错误;C项,饱和BaSO4溶液中c(Ba2+)=![]() =1
=1![]() 10-5mol/L,由于溶液的体积未知,无法计算Ba2+物质的量,错误;D项,Na2O中的阴、阳离子依次为O2-、Na+,1molNa2O中含有阴、阳离子总物质的量为3mol,BaO2中的阴、阳离子依次为O22-、Ba2+,1molBaO2中含有阴、阳离子总物质的量为2mol,1molNa2O和BaO2混合物中含有的阴、阳离子总物质的量在2mol~3mol之间,错误;答案选A。
10-5mol/L,由于溶液的体积未知,无法计算Ba2+物质的量,错误;D项,Na2O中的阴、阳离子依次为O2-、Na+,1molNa2O中含有阴、阳离子总物质的量为3mol,BaO2中的阴、阳离子依次为O22-、Ba2+,1molBaO2中含有阴、阳离子总物质的量为2mol,1molNa2O和BaO2混合物中含有的阴、阳离子总物质的量在2mol~3mol之间,错误;答案选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应2NO2 ![]() 2NO+O2 , 在体积固定的密闭容器中反应,达到平衡状态的标志是( )
2NO+O2 , 在体积固定的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2 , 同时生成2n mol NO2;
②单位时间内生成n mol O2 , 同时生成2n mol NO;
③NO2、NO、O2的浓度比为2:2:1;
④混合气体的压强不再改变;
⑤混合气体的颜色不再改变;
⑥混合气体的平均摩尔质量不再改变.
A.①④⑤⑥
B.①②③⑤
C.②③④⑥
D.以上全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
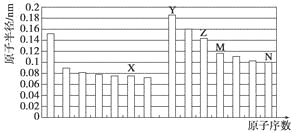
A. Z、N两种元素的离子半径相比,前者较大
B. X、N两种元素的气态氢化物的沸点相比,前者较低
C. 由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两个热化学方程式中,△H1 和△H2的相对大小正确的是( ) S(s)+O2(g)=SO2(g)△H1; S(g)+O2(g)=SO2(g)△H2 .
A.△H1>△H2
B.△H1<△H2
C.△H1﹦△H2
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含48.6% 的SiO2、16.2% 的ZnO、19.4% 的ZnS 和12 .8% 的CuS 及少量的Fe3O4。.某同学用10.0g该废催化剂为原料,回收锌和铜。采用的实验方案如下,回答下列问题:

已知:金属Zn 与Al类似,都是两性金属,能溶于强碱并放出氢气,但铝不溶于氨水,锌却可以溶于氨水形成四氨合锌配离子[Zn(NH3)4]2+。
(1)滤液1中含有Fe2+,选用提供的试剂进行检验,检验方法如下:__________________________。(提供的试剂:稀盐酸、KSCN 溶液、KMnO4 溶液、NaOH 溶液、K3[Fe(CN)6]溶液)
(2)滤渣2 除SiO2 外的另一成分是____________;第二次浸出时,加热温度不宜过高的原因是___________________;写出第二次浸出的化学反应方程式____________________________________。写出锌溶于氨水的离子方程式____________________________________。
(3)ZnSO4在水中的溶解度,随温度的升高而缓慢增大,从硫酸锌溶液得到七水硫酸锌晶体,可采用的方法是_____________________;析出七水硫酸锌晶体,减压过滤,用于淋洗七水硫酸锌晶体的溶剂是___________________;某同学在实验完成之后,得到5.74gZnSO4·7H2O(式量287)则锌的回收率为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象涉及焰色试验的是
A.硝石(KNO3)强烧之,紫青烟起
B.绿蚁新醅酒,红泥小火炉
C.一道残阳铺水中,半江瑟瑟半江红
D.日照香炉生紫烟,遥看瀑布挂前川
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用滴有酚酞和氯化钠溶液的湿润滤纸分别做甲、乙两个实验,下列判断正确的是

A. b、d两极附近均有气泡冒出
B. 甲乙中变红色的电极均发生了还原反应
C. a、d两极电极反应均为:Fe-2e-=Fe2+
D. 乙中铁棒比甲中铁棒更易腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存并且溶液为无色透明的离子组是( )
A. Ba2+、Na+、NO3-、SO42-B. Mg2+、Cl-、Al3+、SO42-
C. K+、Cl-、CO32-、NO3-D. Ca2+、Na+、Fe3+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用硝酸和废铜屑(含Cu和CuO)作为原料制备硝酸铜,设计的流程如下:
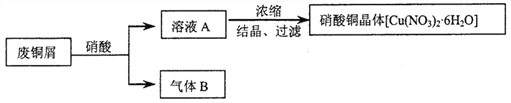
(1)某次实验使用了废铜屑共24g,用一定浓度的硝酸100mL完全溶解这些废铜屑时,共收集到标准状况下B气体6.72L(其中NO2和NO的体积比为2∶1)。请通过计算回答下列问题:
①废铜屑中铜和氧化铜的物质的量之比_____________。
②若测得溶液A中H+的浓度为1mol·L-1,则原硝酸的物质的量浓度为________________。(假设反应前后溶液的体积不变)
(2)上述制备方案中产生的气体B,既造成原料的浪费,也污染了环境。请你设计方案解决上述问题___________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com