
科目:高中化学 来源: 题型:选择题
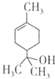
| A. | 1mol该物质最多能和lmol氢气发生加成反应 | |
| B. | 该物质属于烃的衍生物 | |
| C. | 该物质能使溴水褪色 | |
| D. | 分子式为C10H20O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
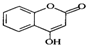 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: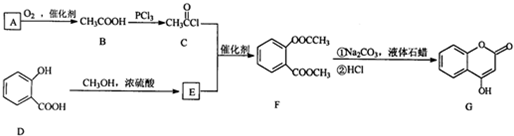
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
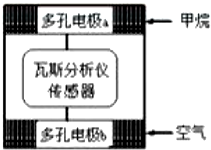 瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 Y2O3-Na2O,O2-可以在其中自由移动.下列有关叙述正确的是( )| A. | 瓦斯分析仪工作时,电池内电路中电子由电极b 流向电极a | |
| B. | 电极b 是正极,O2-由电极 a流向电极b | |
| C. | 电极a的反应式为:CH4+4O2--8e-=CO2+2H2O | |
| D. | 当固体电解质中有1 mol O2- 通过时,电子转移 4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
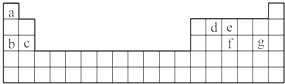
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 浓度 时间(秒) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
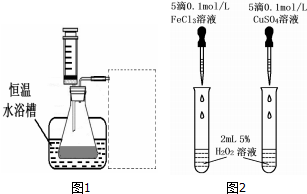
| 所需试剂 | 操作及现象 | 结论 |
| Cl对H2O2分解无催化作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com