
��֪A��g��+B��g��⇌C��g��+D��g����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/�� 700 800 830 1000 1200
ƽ�ⳣ�� 1.7 1.1 1.0 0.6 0.4
830��ʱ����һ��2L���ܱ������г���0.2mol��A��0.8mol��B����Ӧ��ʼ4s��A��ƽ����Ӧ����v��A��=0.005mol/��L•s��������˵����ȷ���ǣ���
A�� 4sʱc��B��Ϊ0.76mol/L
B�� 830���ƽ��ʱ��A��ת����Ϊ80%
C�� ��Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
 D�� 1200��ʱ��ӦC��g��+D��g��⇌A��g��+B��g����ƽ�ⳣ����ֵΪ0.
D�� 1200��ʱ��ӦC��g��+D��g��⇌A��g��+B��g����ƽ�ⳣ����ֵΪ0. 4
4
���㣺 ��ѧƽ�⽨���Ĺ��̣���ѧƽ���Ӱ�����أ�
ר�⣺ ��ѧƽ��ר�⣮
������ A���ȸ�������֮�ȵ��ڻ�ѧ������֮�����v��B����Ȼ����ݡ�c=v��t�����c��B����B����ʼŨ��﹣��c��A��=4sʱc��B����
B����ƽ��ʱA��Ũ�ȱ仯��Ϊx����������ʽ��ʾƽ��ʱ����ֵ�ƽ��Ũ�ȣ�����ƽ�ⳣ���з��̼���x��ֵ���ٸ���ת���ʶ�����㣻
C���ɱ����֪���¶����ߣ���ѧƽ�ⳣ����С��ƽ�������ƶ���
D���÷�ӦC��g��+D��g��⇌A��g��+B��g����A��g ��+B��g��⇌C��g��+D��g���෴����ƽ�ⳣ����Ϊ������
��+B��g��⇌C��g��+D��g���෴����ƽ�ⳣ����Ϊ������
��� �⣺A����Ӧ��ʼ4s��A��ƽ����Ӧ����v��A��=0.005mol/��L•s��������֮�ȵ��ڻ�ѧ������֮�ȣ�����v��B��=v��A��=0.005mol/��L•s������4s�ڡ�c��B��=0.005mol•L﹣1•s﹣1��4s=0.02mol/L��B����ʼŨ��Ϊ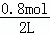 =0.4mol/L����4sʱc��B��=0.4mol/L﹣0.02mol/L=0.38mol/L����A����
=0.4mol/L����4sʱc��B��=0.4mol/L﹣0.02mol/L=0.38mol/L����A����
B����ƽ��ʱA��Ũ�ȱ仯��Ϊx����
A��g��+B��g��⇌C��g��+D��g��
��ʼ��mol/L����0.1 0.4 0 0
�仯��mol/L����x x x x
ƽ�⣨mol/L����0.1﹣x 0.4﹣x x x
�� =1�����x=0.08
=1�����x=0.08
����ƽ��ʱA��ת����Ϊ ��100%=80%����B��ȷ��
��100%=80%����B��ȷ��
C���ɱ����֪���¶����ߣ���ѧƽ�ⳣ����С��ƽ�������ƶ������������ƶ�����C����
D.1200��ʱ��ӦA��g��+B��g��⇌C��g��+D��g����ƽ�ⳣ��ֵΪ0.4������1200��ʱ��ӦC��g��+D��g��⇌A��g��+B��g����ƽ�ⳣ����ֵΪ =2.5����D����
=2.5����D����
��ѡB��
������ ���⿼�黯ѧ��Ӧ���ʡ���ѧƽ�ⳣ���ļ��������õȣ��ѶȽϴ�ע���¶Ȳ���ʱ��ƽ�ⳣ�����䣬��ѧ����ʽ�෴ʱ��ƽ�ⳣ����Ϊ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ӦX��g��+Y��g��⇌2Z��g������H��0���ﵽƽ��ʱ������˵����ȷ���ǣ���
A�� ��С���������ƽ�������ƶ�
B�� ���������Z�IJ�������
C�� ����c��X����X��ת��������
D�� �����¶ȣ�Y��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���������У�������ʵ�ʵ��ǣ���
A�� ҽ��ҩƷӦ�ڵ��¡�����Ļ������ܷⱣ��
B�� ��Ӧ�е�ijһ���ʵ�ת���ʦ���B��������÷�Ӧ��ƽ�ⳣ��Kһ������
C�� ��һ�����𡰹ķ硱��������������ȼ����ȥ
D�� ����MnO2��ĩ����ʹ����������ٷֽ⣬��MnO2�������ڷ�Ӧǰ��û�����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ѧ��ȤС��ѧϰԭ���֪ʶ��������ԭ���������������ۡ�����̿�����ε����ʿ�����Ʒ��С�������������ԭ�������ⲻ��ȷ���ǣ���
A�� �����Ƴ�С��װ���ڸ���������
B�� ���÷�Ӧ�ų�������ԭ���Ƴ�ů����
C�� ������ؽṹ���ɽ����¶ȣ��������ӳ���㱣����
D�� �����ĵ缫��ӦΪ��2H2O+O2+4e﹣=4OH﹣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ڷ�������ԭ��Ӧ���ǣ�������
| �� | A�� | C+O2 |
| �� | B�� | CaCO3+2HCl=CaCl2+CO2��+H2O |
| �� | C�� | 2Na2O2+2H2O=4NaOH+O2�� |
| �� | D�� | Zn+H2SO4=ZnSO4+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ�������뽺�������ص��ǣ�������
| �� | A�� | ��е�FeCl3��Һ��ȴ����һ�������䣬��һ��������ͨ· |
| �� | B�� | ��������������ˮ |
| �� | C�� | ��̬�����������ɢ�ڲ������Ƴ���ɫ���� |
| �� | D�� | ���Ȼ�����Һ�м���NaOH��Һ���ֺ��ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ��ݴ�����˵����ȷ���ǣ�������

| �� | A�� | ����������ʵ���Ũ��Ϊ9.2 mol/L |
| �� | B�� | ����������������ˮ��ϣ�������Һ����������С��49% |
| �� | C�� | ��ʵ������Ҫ4.6 mol/L��ϡ����480 mL����Ӧ����Ͳ��ȡ������125.0mL |
| �� | D�� | ��������ˮ���������������Һ�����ʵ���Ũ�ȴ���9.2 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������ڵ���ʵ��ǣ�������
���Ȼ��� ��NH3•H2O ��������Һ ������ �ݶ�����̼��
| �� | A�� | �٢� | B�� | �٢ܢ� | C�� | �٢ڢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com