
| A. | 实验室用溴水和苯在催化剂作用下制溴苯: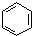 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$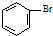 +HBr +HBr | |
| B. | 乙酸乙酯和H${\;}_{2}^{18}$O发生酸性水解反应:CH3COOC2H5+H-18OH $?_{△}^{酸}$CH3CO18OH+C2H5OH | |
| C. | 苯酚钠溶液中通入少量二氧化碳的离子方程式:2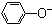 +CO2+H2O→ +CO2+H2O→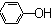 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 甲醛溶液与足量的银氨溶液共热:HCHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$HCOONH4+2Ag↓+3NH3+H2O |
分析 A.苯与溴水不反应;
B.酯水解生成酸和醇,水中的${\;}_{2}^{18}$O存在于酸中;
C.苯酚钠溶液中通入少量二氧化碳生成碳酸氢钠;
D.甲醛溶液与足量的银氨溶液反应生成碳酸铵.
解答 解:A.苯与溴水不反应,在催化作用下与液溴反应,故A错误;
B.酯水解生成酸和醇,水中的${\;}_{2}^{18}$O存在于酸中,方程式为CH3COOC2H5+H-18OH $?_{△}^{酸}$CH3CO18OH+C2H5OH,故B正确;
C.苯酚钠溶液中通入少量CO2的离子反应为CO2+H2O+C6H5O-→C6H5OH+HCO3-,故C错误;
D.醛溶液与足量的银氨溶液共热的离子反应为HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O,故D错误.
故选B.
点评 本题考查较综合,涉及离子反应方程式书写的正误判断、混合物分离提纯、有机物的结构与性质等,注重高频考点的考查,把握发生的反应及离子反应的书写方法、有机物的性质等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
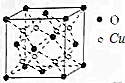 科学家研究发现金属离子吸收氧气的能力十分巨大,人体血液中的血红蛋白依靠亚铁离子结合氧气,其他金属离子(Cu2+、Zn2+等)也可以实现结合和运输氧气的目的.最近丹麦科学家研发了一种晶体材料,该晶体吸收氧气的能力依靠钴离子,它可以让人在水下持久地获得氧气.
科学家研究发现金属离子吸收氧气的能力十分巨大,人体血液中的血红蛋白依靠亚铁离子结合氧气,其他金属离子(Cu2+、Zn2+等)也可以实现结合和运输氧气的目的.最近丹麦科学家研发了一种晶体材料,该晶体吸收氧气的能力依靠钴离子,它可以让人在水下持久地获得氧气.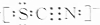 ,则SCN-中σ 键与π键的个数比为1:1.
,则SCN-中σ 键与π键的个数比为1:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素水解的最终产物都是葡萄糖 | |
| B. | 误服可溶性重金属盐,立即服用大量牛奶可以解毒 | |
| C. | 用灼烧的方法可鉴别毛织物和棉织物 | |
| D. | 温度越高,酶对某些化学反应的催化效率越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应A(s)?2B(g)+C(g),当C的体积分数不变时,反应达到平衡状态 | |
| B. | 将钢闸门与直流电源的正极相连,可防止钢闸门腐蚀 | |
| C. | 用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+Hg2+(aq)═HgS(s)+Fe2+(aq) | |
| D. | 增大反应物浓度可加快反应速率,因此可用浓硫酸与铁反应增大生成氢气的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液的pH值不变 | B. | 溶液中Na2CO3的物质的量不变 | ||
| C. | Na+与CO32-数目不变 | D. | Na2CO3溶液的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强,平衡常数将增大 | |
| B. | 达到平衡时,单位时间里消耗n mol S2Cl2的同时也生成n molCl2 | |
| C. | 达到平衡时,若升高温度,氯气的百分含量减小 | |
| D. | 加入氯气,平衡向正反应方向移动,氯气的转化率一定升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
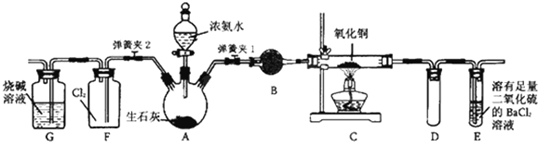
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 基态Mg原子的核外电子排布图: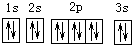 | |
| B. | 过氧化氢的电子式: | |
| C. | As原子的简化电子排布式:[Ar]4s24p3 | |
| D. | 羟基的电子式: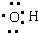 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com