
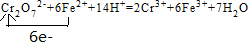 .
.分析 (1)Fe元素的化合价升高,Cr元素的化合价降低,结合电子、电荷守恒分析;
(2)Fe(Ⅱ)[Fe(Ⅲ)xCr2-x]O4中正负化合价的倒数和为0;
(3)类似铝离子与碱的反应,由此分析解答.
解答 解:(1)Fe2+还原Cr2O72-的离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,Fe失去电子,Cr得到电子,该反应转移6e-,电子转移的方向和数目为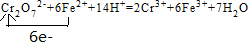 ,
,
故答案为: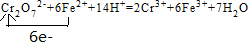 ;
;
(2)Fe(Ⅱ)[Fe(Ⅲ)xCr2-x]O4中正负化合价的倒数和为0,则+2+3x+3×(2-x)+(-2)×4=0,解得x=1.5,故答案为:1.5;
(3)Cr3+在过量的NaOH溶液中会转化为CrO2-,这一转化的离子方程式为Cr3++4OH-=CrO2-+2H2O,由此可知Cr(OH)3呈两性,
故答案为:Cr3++4OH-=CrO2-+2H2O;两.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意电子守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 100 mL 0.2 mol/L 氯化钾溶液 | B. | 200 mL 0.1 mol/L 硝酸钾溶液 | ||
| C. | 100 mL 0.1 mol/L 硝酸钾溶液 | D. | 50 mL 0.2 mol/L 磷酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
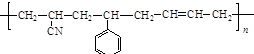 除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2.
除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2. )需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.
)需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.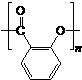 .
.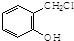 制备A的合成路线.
制备A的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
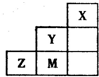
| A. | Y、Z可形成ZY6分子 | B. | X晶体属于原子晶体 | ||
| C. | 原子半径:Z>M>Y | D. | Z离子的结构示意图可表示为: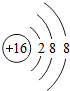 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 770 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
| A. | 甲组和乙组的实验中,盐酸均是过量的 | |
| B. | 盐酸的物质的量浓度为0.8mol•L-1 | |
| C. | 合金中镁铝的物质的量之比为1:1 | |
| D. | 丙组中铝的物质的量为0.015mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜粉溶解于1L0.5mol•L-1稀硝酸中,当生成2.24LNO时,溶液中氮原子数为0.4 NA | |
| B. | 标准状况下,22.4LSO3的分子数为NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,生成了0.2molO2,转移电子的数目为0.8 NA | |
| D. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com