
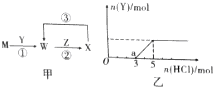
分析 (1)若M为短周期常见金属单质,W、X均为含M元素的盐,且W溶液的pH>7.说明M元素可形成酸根离子,则应为Al,则W含有AlO2-,X应含有Al3+;
(2)若M是浅黄色化合物,应为Na2O2,常温下Y是无色气体,应为CO2;X中含有的阴、阳离子均为10电子粒子,应为NaOH;
(3)若将(2)中的气体Y通入氢氧化钡溶液中得到不溶物N,N为BaCO3.
解答 解:(1)若M为短周期常见金属单质,W、X均为含M元素的盐,且W溶液的pH>7.说明M元素可形成酸根离子,则应为Al,则W含有AlO2-,X应含有Al3+,则Y为强碱,偏铝酸钠溶液水解呈碱性,方程式为AlO2-+2H2O?Al(OH)3+OH-,反应③的离子方程式为Al3++4OH-=2H2O+AlO2-,
故答案为:碱(强碱);AlO2-+2H2O?Al(OH)3+OH-;Al3++4OH-=2H2O+AlO2-;
(2)若M是浅黄色化合物,应为Na2O2,常温下Y是无色气体,应为CO2;X中含有的阴、阳离子均为10电子粒子,应为NaOH,含有(极性)共价键、离子键,
分析图乙,3~5的反应为HCO3-+H+=CO2↑+H2O,此时消耗盐酸2mol,1~3肯定发生CO32-+H+=HCO3-,该反应应消耗2molHCl,而此时消耗3molHCl,则肯定含有NaOH,
反应至a点溶液为NaHCO3,溶液呈碱性,存在离子浓度:c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),
故答案为:(极性)共价键、离子键;NaOH、Na2CO3;c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);
(3)若将(2)中的气体Y通入氢氧化钡溶液中得到不溶物N,N为BaCO3,现将该沉淀放入0.1mool/L的BaCl2溶液中,其Ksp不变,只受温度的影响,
c(CO32-)=$\frac{8.1×1{0}^{-9}}{0.1}$mol/L=8.1×10-8mol/L.
故答案为:不变;8.1×10-8.
点评 本题以元素化合物的推断为载体考查了元素化合物的性质,同时考查学生分析问题、解决问题的能力,明确物质的性质是解本题的关键,难度不大.


科目:高中化学 来源: 题型:解答题
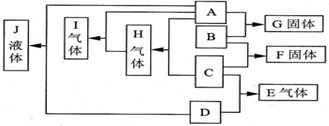
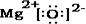 ,其化学键的类型为离子键.
,其化学键的类型为离子键.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
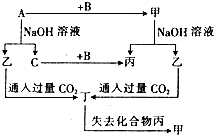 由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题:
由短周期元素组成的单质A、B、C和四种化合物甲、乙、丙、丁有如图所示的转化关系,已知C是密度最小的气体,甲是电解质.根据图示转化关系回答问题: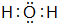 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
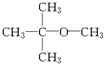 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素元素都有正化合价 | B. | 卤素元素的单质都只具有氧化性 | ||
| C. | 卤素元素的最低化合价都是-1价 | D. | 卤素元素氢化物都是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
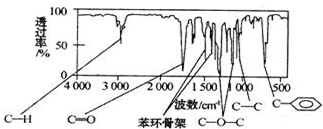
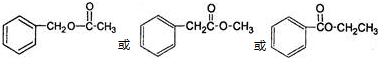 .(任写一种)
.(任写一种)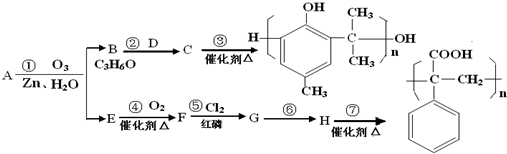
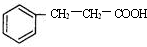 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③①④ | B. | ③②①④ | C. | ③①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚氯乙烯塑料强度大,抗腐蚀性强,可以用来包装需长时间保存的食品 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 油脂、淀粉、纤维素、蛋白质都属于天然有机高分子材料 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
 现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请列式计算,
现有一瓶葡萄糖(C6H12O6)溶液,部分标签如图所示,请列式计算,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com