


科目:高中化学 来源: 题型:
 下面给出了四种烃A、B、C、D的相关信息:
下面给出了四种烃A、B、C、D的相关信息:查看答案和解析>>
科目:高中化学 来源: 题型:
 利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.
利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是干冰的晶胞结构示意图.请完成下列问题:
如图是干冰的晶胞结构示意图.请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
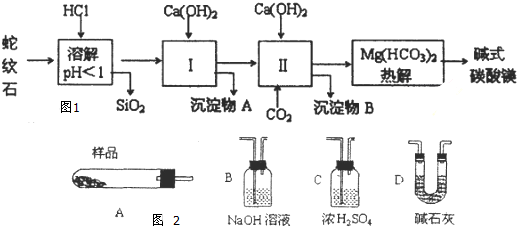
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.9 | 3.3 | 9.4 |
沉淀完全时PH | 3.2 | 5.4 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
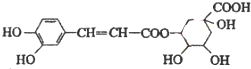
| A、分子式为C16H15O9 |
| B、不能与NaHCO3溶液反应 |
| C、能发生取代反应和消去反应 |
| D、1 mol绿原酸最多与可8mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
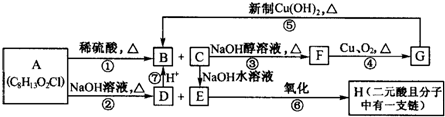
查看答案和解析>>
科目:高中化学 来源: 题型:
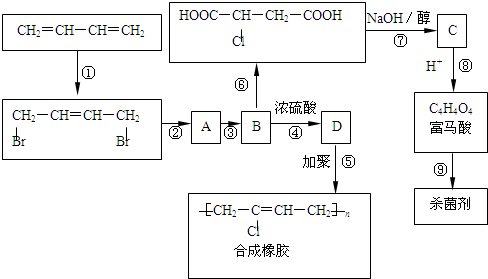
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com