
| A£®ĢśŌŚĄäµÄÅØĮņĖįÖŠŗĶĀĮŌŚĄäµÄÅØĻõĖįÖŠ¶¼Ć»ÓŠĆ÷ĻŌ±ä»Æ |
| B£®ÅØĮņĖįŗĶÅØŃĪĖį³¤ĘŚ±©Ā¶ŌŚæÕĘųÖŠÅØ¶Č½µµĶ |
| C£®SO2”¢ĘÆ°×·Ū”¢»īŠŌĢ攢¹żŃõ»ÆÄʶ¼ÄÜŹ¹ŗģÄ«Ė®ĶŹÉ« |
| D£®ĘÆ°×·ŪŗĶĖ®²£Į§³¤ĘŚ±©Ā¶ŌŚæÕĘųÖŠ±äÖŹ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
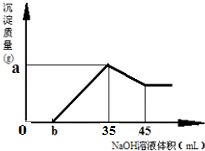
| A£®0.5 mol/L | B£®3.0 mol/L |
| C£®2.0 mol/L | D£®1.0 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
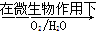 Fe2++SO42-
Fe2++SO42-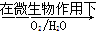 Fe3+
Fe3+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
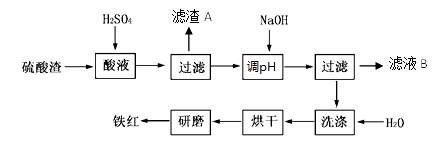
| ³ĮµķĪļ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| æŖŹ¼³Įµķ | 2.7 | 3.8 | 7.5 | 9.4 |
| ĶźČ«³Įµķ | 3.2 | 5.2 | 9.7 | 12.4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓĆFeCl3ČÜŅŗøÆŹ“ĶÖĘÓ”Ė¢µēĀ·°å£ŗFe3£«£«Cu=Fe2£«£«Cu2£« |
| B£®NH4HCO3ČÜŅŗŗĶ¹żĮæµÄNaOHČÜŅŗĻą»ģŗĻ£ŗHCO3”Ŗ£«OH£=CO32”Ŗ£«H2O |
| C£®ĻņFe2(SO4)3µÄĖįŠŌČÜŅŗÖŠĶØČė×ćĮæH2S£ŗFe3£«£«H2S=FeS”ż£«2H£« |
| D£®FeI2ČÜŅŗÖŠĶØČėCl2ÖĮI£Ē”ŗĆĶźČ«±»Ńõ»Æ£ŗ2I££«Cl2=I2£«2Cl£ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com