
分析 电解质是指:在水溶液或熔化状态下都能导电的化合物;单质,混合物既不是电解质也不是非电解质.
(1)强电解质是指在水溶液中,或熔融状态下能完全电离的化合物;
(2)弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐;
(3)在水溶液中和熔化状态下都不能导电的化合物是非电解质;
(4)酸性氧化物是和碱反应生成盐和水的氧化物;
(5)酸式盐是多元酸部分被碱中和反应生成的盐;
(6)分散系是一种或多种物质分散到另一种物质中形成的混合物.
解答 解:(1)水溶液中,或熔融状态下能完全电离的化合物有⑤硫酸钡 ⑥碳酸氢钠 ⑨醋酸铵,
故答案为:⑤⑥⑨;
(2)在水溶液里部分电离的电解质④醋酸,
故答案为:④;
(3)在水溶液中和熔化状态下都不能导电的化合物有①液氨,⑦二氧化氮,⑧二氧化碳,⑩葡萄糖,
故答案为:①⑦⑧⑩;
(4)和碱反应生成盐和水的氧化物有⑧二氧化碳为酸性氧化物,
故答案为:⑧;
(5)属于酸式盐的有⑥碳酸氢钠,
故答案为:⑥;
(6)属于分散系的是②氨水 ③盐酸,
故答案为:②③.
点评 本题是对基本概念的考查,注意电解质、非电解质概念的辨析以及与导电的关系是解答的关键,平时注意基础知识的积累,题目难度不大.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 该温度下的平衡常数是:K=$\frac{9}{16}$ | |
| B. | 达到平衡时,NO的转化率是60% | |
| C. | 3min末达到平衡,则v(NO)=0.01mol/(L•min) | |
| D. | 升高温度有利于活性炭处理更多的污染物NO |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
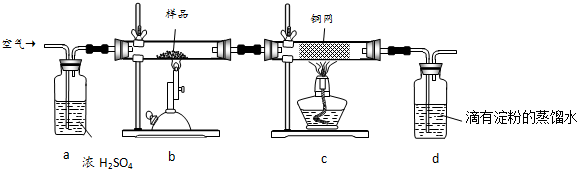

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 过氧化钠和水反应:2O22-+2H2O=4OH-+O2↑ | |
| B. | 含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 硫化钠水溶液呈碱性:S2-+H2O?HS-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中的少量HCl:通入NaOH溶液 | |
| B. | 除去KCl溶液中的少量K2CO3:加入适量的盐酸 | |
| C. | 向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42- | |
| D. | 用BaCl2溶液,可将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
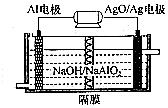 (1)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应为FeO42-+3eˉ+4H2O=Fe(OH)3+5OH-,该电池总反应的离子方程式为3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.
(1)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应为FeO42-+3eˉ+4H2O=Fe(OH)3+5OH-,该电池总反应的离子方程式为3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com