
| A. | 常温常压下,3.0 g乙烷中含有的碳氢键数为0.6NA | |
| B. | 标准状况下,22.4 L C2H5OH中含有的氢原子数为6 NA | |
| C. | 常温常压下,92 g的 NO2和N2O4混合气体含有的分子数为 6 NA | |
| D. | 标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5 NA |
分析 A.质量换算物质的量结合乙烷分子结构计算碳氢键数;
B.标准状况下,乙醇是液体;
C. NO2的分子量为46,N2O4的分子量为92;
D.过氧化钠自身氧化还原反应每2mol过氧化钠反应生成1mol氧气,转移电子2mol.
解答 解:A.3.0 g乙烷物质的量=$\frac{3.0g}{30g/mol}$=0.1mol,含有的碳氢键数=0.1mol×6=0.6mol,故A正确;
B.标准状况下,22.4 L C2H5OH物质的量不是1mol,故B错误;
C.不知道NO2和N2O4的具体含量,无法计算,故C错误;
D.过氧化钠自身氧化还原反应每2mol过氧化钠反应生成1mol氧气,转移电子2mol,由Na2O2制得11.2 L O2,反应转移的电子数为NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常的应用,主要考查质量、物质的量、微粒数的关系,气体摩尔体积的体积应用,氧化还原反应的电子转移应用,题目难度中等.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℉、30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |
| D. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应△H=+2×283.0 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 ; B
; B ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10Q | B. | 5Q~10Q | C. | 3Q | D. | 8Q |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱沾在皮肤上立即抹上稀硫酸 | |
| B. | “油锅”着火用锅盖或湿布盖灭 | |
| C. | 浓硫酸沾在皮肤上,先用干布或用纸吸干,再用大量清水冲洗 | |
| D. | 发生CO中毒时,首先采取开门、窗通风的措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
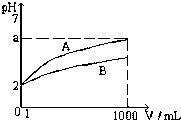 T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示
T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com