
| A. | 吸热反应是由于反应物的总能量比生成物的总能量低 | |
| B. | 放热反应的△H<0 | |
| C. | 需要加热才能发生反应一定是吸热反应 | |
| D. | 酸碱中和反应都是放热反应 |
分析 A.反应物的总能量比生成物的总能量低,发生反应时吸收能量;
B.放热反应的焓变为负;
C.吸热、放热与反应条件无关;
D.中和反应放出热量.
解答 解:A.反应物的总能量比生成物的总能量低,发生反应时吸收能量,则为吸热反应,故A正确;
B.放热反应的焓变为负,则放热反应的△H<0,故B正确;
C.吸热、放热与反应条件无关,如C与二氧化碳的反应为吸热反应,Fe与氯气加热发生的反应为放热反应,故C错误;
D.中和反应放出热量,则酸碱中和反应都是放热反应,故D正确;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | “绿色化学”的核心是应用化学原理对环境污染进行治理 | |
| B. | “火树银花”中的焰火实质上是金属元素的焰色反应 | |
| C. | 李白有诗云“日照香炉生紫烟”这是描写“碘的升华” | |
| D. | 煤经过气化、液化和干馏等物理变化过程,可以转化为清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠是银白色、质软、熔点相对较低、密度比水小的金属单质 | |
| B. | 大量的钠着火时可以用沙子扑灭 | |
| C. | 金属钠在空气中长期放置,最终变为碳酸钠 | |
| D. | 过氧化钠是白色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 正极为Cu,负极为Fe,电解质为FeCl3溶液 | |
| B. | 正极为C,负极为Fe,电解质为Fe(NO3)3溶液 | |
| C. | 正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液 | |
| D. | 正极为Ag,负极为Fe,电解质为CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaBr全部转化为NaCl | B. | 10.3g NaBr参加了反应 | ||
| C. | 50%的Br-离子被还原 | D. | 16.15g固体由NaCl、NaBr和Br2组成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中不一定含有SO42- |
| B | FeCl2溶液中,滴加KSCN溶液和溴水 | 滴加KSCN溶液,无明显变化;滴加溴水后,溶液变为血红色 | 氧化性:Br2>Fe3+ |
| C | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| D | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
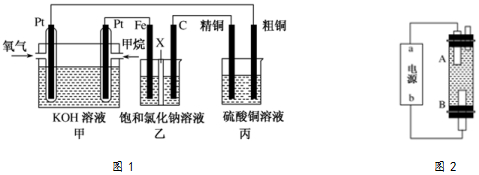
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com