
【题目】在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K 和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =_____________________。
(2)该反应为____________反应(选填“吸热”、“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_____________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 _________。
(5)1200℃时,在2L的密闭容器中,反应开始时加入1mol CO2、1mol H2、2molCO、2mol H2O,则反应向__________进行(填“正方向”、“逆方向”或“不移动”)
【答案】![]() 吸热 bc 830℃ 逆方向
吸热 bc 830℃ 逆方向
【解析】
(1)平衡常数为生成物浓度幂之积与反应物浓度幂之积的比;
(2)根据温度升高,平衡常数变大来分析;
(3)利用平衡的特征“等”和“定”来分析;
(4)根据浓度和平衡常数来计算平衡常数,从而确定温度;
(5)比较QC与K的相对大小,如果QC>K逆向移动,QC═K,不移动,QC<K正向移动。
(1)平衡常数为生成物浓度幂之积与反应物浓度幂之积的比,则CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K=
CO(g)+H2O(g)的平衡常数K=![]() ;
;
(2)由温度升高,平衡常数变大可知,升高温度,平衡向正反应方向移动,则正反应为吸热反应;
(3)a.该反应为气体的总物质的量不变的反应,则容器中压强始终不变,不能作为判定平衡的方法,故A错误;
b.混合气体中c(CO)不变,则达到化学平衡,故B正确;
c.V(H2)正=V(H2O)逆,则对于氢气来说正、逆反应速率相等,此时反应达到平衡,故C正确;
d.c(CO2)=c(CO),该反应不一定达到平衡,浓度关系取决于反应物的起始量和转化率,故D错误;
故答案为:bc;
(4)c(CO2)c(H2)=c(CO)c(H2O)时,平衡常数K=![]() =1,则该温度为830℃;
=1,则该温度为830℃;
(5)1200℃时,在2L的密闭容器中,反应开始时加入1mol CO2、1mol H2、2molCO、2mol H2O,Qc=![]() =
=![]() =4>2.6,说明反应逆方向进行。
=4>2.6,说明反应逆方向进行。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】25℃、101KPa时,agNH3与bgCH4的体积相同,下列叙述不正确的是
A.NH3、CH4的物质的量之比为a: b
B.NH3、CH4两种气体的密度之比为a: b
C.NH3、CH4的摩尔质量之比为17: 16
D.NH3、CH4的分子数之比为1 : 1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芬必得是葛兰素史克公司的止痛药品牌,目前在中国由合资公司中美史克运营,在国内有四款主要止痛产品。芬必得布洛芬缓释胶囊是芬必得止痛系列产品之一,布洛芬为该类止痛药的通用名称,下列有关芬必得的说法正确的是
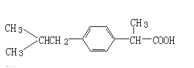
A.分子式为![]() ,分子中含有两种官能团
,分子中含有两种官能团
B.最多12个原子共平面
C.可以跟Na、Na2CO3、NaHCO3反应也可以和![]() 在一定条件下反应
在一定条件下反应
D.可以通过化学反应使溴水和酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示(不考虑CO2的溶解)。下列判断正确的是
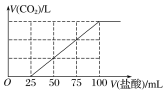
A.原NaOH溶液的浓度为0.2 mol/L
B.通入CO2在的体积为336 mL
C.所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3
D.所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C常温下为一种液体,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,F为棕黄色溶液。①是实验室制取丁的反应之一。各物质间的转化如下图所示,回答下列问题(部分生成物未列出):

(1)物质I的化学式为________;
(2)在反应①中,当生成标准状况下丁气体4.48L时,反应转移的电子数约为___________;
(3)B与K的反应是实验室制取丙的反应,其离子方程式为________________;
(4)反应②的化学方程式为_____________;
(5)若E与G以物质的量比为1:1投入足量水中,反应的离子方程式为________;
(6)写出实验室检验F中阴离子的方法_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】秸秆(含多糖物质)的综合应用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
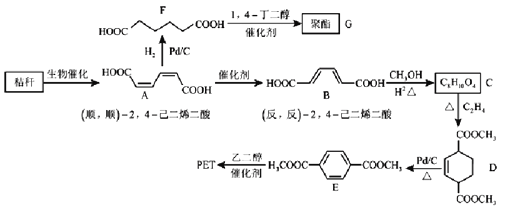
回答下列问题:
(1)下列关于糖类的说法正确的是______________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为______。
(3)D中官能团名称为______,D生成E的反应类型为______。
(4)F 的化学名称是______,由F生成G的化学方程式为______。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成44 gCO2,W共有______种(不含立体结构),其中核磁共振氢谱为三组峰的结构简式为_________。
(6)参照上述合成路线,以(反,反)-2,4-己二烯和C2H4为原料(无机试剂任选),设计制备对二苯二甲酸的合成路线_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2=CH2 ③![]() ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4
A. ①②③B. ①②④C. ③④⑤D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.25℃时,测得一元酸HA溶液pH=3,则HA一定为弱电解质
B.25℃时,将0.05mol·L-1的H2SO4溶液加水稀释100倍,所得溶液的pH=3
C.25℃时,将0.1mol·L-1的一元碱BOH溶液加水稀释至pH=9,所得溶液![]()
D.25℃时,pH=11的一元碱BOH溶液与pH=3的HA溶液等体积混合,所得溶液pH可能为7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com