
科目:高中化学 来源:2012届湖南省湖南师大附中高三第三次月考化学试卷 题型:填空题
(8分)常温下已知pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性;0.01mol·L-1的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性。请回答下列问题:
(1)高碘酸是 (填“强酸”或“弱酸”)
(2)0.01mol·L-1的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合所得溶液中IO—3与Na+的物质的量的关系是n(Na+) n(IO-3)(填“大于”、“小于”或“等于”)。
(3)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸、碘酸和硫酸,此反应的还原剂是 ,该反应的离子方程式可表示为 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖南省高三第三次月考化学试卷 题型:填空题
(8分)常温下已知pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性;0.01mol·L-1的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性。请回答下列问题:
(1)高碘酸是 (填“强酸”或“弱酸”)
(2)0.01mol·L-1的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合所得溶液中IO—3与Na+的物质的量的关系是n(Na+) n(IO-3)(填“大于”、“小于”或“等于”)。
(3)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸、碘酸和硫酸,此反应的还原剂是 ,该反应的离子方程式可表示为 。
查看答案和解析>>
科目:高中化学 来源:2010年江西省高二上学期期中考试化学卷 题型:填空题
(10分)常温下已知pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性;0.01mol·L-1的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性。请回答下列问题:
(1)高碘酸是 (填“强酸”或“弱酸”),理由是 。
(2)0.01mol·L-1的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合所得溶液中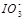 与Na+的浓度关系是
(填“大于”“小于”或“等于”)。
与Na+的浓度关系是
(填“大于”“小于”或“等于”)。
(3)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸、碘酸和硫酸,此反应的还原剂是 ,该反应的离子方程式可表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
( 12分)
I.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验编号 | HA物质的量浓度 | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸______________________________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2_______ (填“是”或“否”)。混合液中离子浓度c(A-) _____ c(Na+) ﹝填>、< 或= )
(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”),此溶液中的溶质
水的电离。 A不影响 B抑制 C促进 (填序号)
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。
II.常温下,pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性; 0.01 mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性。请回答下列问题:
(1)高碘酸钾溶液在冰水浴中和常温下,pH前者比后者 (填>、< 或= )
(2)已知高碘酸和硫酸锰在溶液中反应生成高锰酸、碘酸和硫酸,该反应的离子方程式为 。
(3)下列说法正确的是
A. 相同物质的量浓度的碘酸钠溶液和高碘酸钠溶液前者水解程度大
B. 高碘酸的氧化性强于高锰酸
C. 高锰酸的酸性强于高碘酸
D.高碘酸的酸性强于硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com