
分析 (1)将炭转化为水煤气,再完全燃烧,最终燃烧得到二氧化碳与水,根据盖斯定律,反应放出的热量为C燃烧生成二氧化碳放出的热量,由②+③可得:C(s)+O2(g)═CO2(g)△H=-393.5 kJ/mol,据此计算;
(2)已知:⑥CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H1=-726.5 kJ/mol,
③CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ/mol
⑤H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ/mol
根据盖斯定律,③+⑤×2-⑥可得:CO(g)+2H2(g)═CH3OH(l),焓变也进行需要计算.
解答 解:(1)将炭转化为水煤气,再完全燃烧,最终燃烧得到二氧化碳与水,根据盖斯定律,反应放出的热量为C燃烧生成二氧化碳放出的热量,由②+③可得:C(s)+O2(g)═CO2(g)△H=-393.5 kJ/mol,故将2.4g炭转化为水煤气,再完全燃烧,整个过程的△H=-393.5 kJ/mol×$\frac{2.4g}{12g}$=-78.7kJ/mol,
故答案为:-78.7;
(2)已知:⑥CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H1=-726.5 kJ/mol,
③CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ/mol,
⑤H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ/mol,
根据盖斯定律,③+⑤×2-⑥可得:CO(g)+2H2(g)═CH3OH(l),则△H=[-283.0+(-285.8)×2-(-726.5)]kJ/mol=-128.1 kJ/mol,
故答案为:CO(g)+2H2(g)═CH3OH(l)△H=-128.1 kJ/mol.
点评 本题考查反应热有关计算、热化学方程式书写,为高频考点,侧重于学生的分析能力和计算能力的考查,本题注意把握盖斯定律的理解与灵活应用,难度中等.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 丁达尔效应可用于鉴别胶体和溶液 | |
| B. | 胶体粒子的直径在1~100 nm之间 | |
| C. | 胶体一定是混合物 | |
| D. | 将FeCl3稀溶液溶于冷水即可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
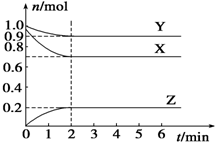 某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应,吸热反应的生成物总能量一定高于反应物总能量 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H不同 | |
| C. | 一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| D. | 一定条件下4 HCl(g)+O2(g)═2Cl2(g)+2H2O(g),当1 mol O2反应放出115.6 kJ热量,键能如下所示,则断裂1 mol H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ Cl2(g)$\stackrel{243kJ/mol}{→}$2Cl(g) O2(g)$\stackrel{498kJ/mol}{→}$2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K1 | 1100 | 841 | 680 | 533 | 409 |
| 起始浓度(mol/L) | 甲 | 乙 | 丙 |
| c(I2) | 0.1 | 0.2 | 0.2 |
| c(I-) | 0.2 | 0.1 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 CH3COOCH2CH3+H2O;反应类型酯化反应.
CH3COOCH2CH3+H2O;反应类型酯化反应.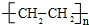 ;反应类型加聚反应.
;反应类型加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 温度 | 初始pH | 0.1mol/L 草酸溶液/mL | 0.01mol/L KMnO4溶的 体积/mL | 蒸馏水 体积/mL | 待测数据(反应混合液褪色 时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | a | b | t3 |
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
| 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com