
| A、Ag | B、Fe | C、Cu | D、K |
| m |
| M |
| 1.6g |
| 32g/mol |


科目:高中化学 来源: 题型:
| A、甲与乙的相对分子质量之比 |
| B、等质量的甲和乙的分子个数之比 |
| C、同温同压下甲与乙的密度之比 |
| D、同温同压下,等质量的甲与乙的压强之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B、电离能最小的电子能量最高 |
| C、同是s能级,在不同的电子层中所能容纳的最多电子数是不相同的 |
| D、核外电子排布完全相同的两种微粒,其化学性质一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
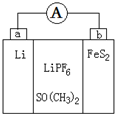 如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )| A、该装置将电能转化为化学能 |
| B、Li+向a极移动 |
| C、可以用水代替SO(CH3)2做溶剂 |
| D、b极反应式是FeS2+4Li++4e-═Fe+2Li2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.0g | B、4g |
| C、4.7g | D、5g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、海水中提取镁的过程中有用到硫酸 |
| B、工业炼铁中加入石灰石的目的是除去铁矿石中的杂质 |
| C、铁、铝常温下不能和浓硫酸、浓硝酸反应 |
| D、铝热反应特指铝与氧化铁的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com