
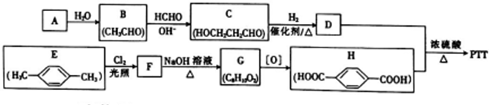
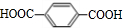
 +n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$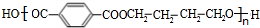 +(2n-1)H2O,该反应的反应类型为缩聚反应.
+(2n-1)H2O,该反应的反应类型为缩聚反应.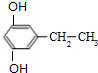 (填结构简式,任写一种)
(填结构简式,任写一种) 分析 A→B(乙醛)是加成反应,则A的分子式为C2H2,结构简式为HC≡CH,乙醛与甲醛发生加成反应生成C,C与氢气发生加成反应生成D为HOCH2CH2CH2OH.由H的结构可知,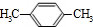 与氯气发生取代反应生成F为
与氯气发生取代反应生成F为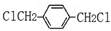 ,G为
,G为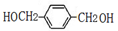 ,F氧化生成
,F氧化生成 ,H与HOCH2CH2CH2OH发生缩聚反应得到PTT为
,H与HOCH2CH2CH2OH发生缩聚反应得到PTT为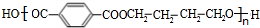 .
.
解答 解:A→B(乙醛)是加成反应,则A的分子式为C2H2,结构简式为HC≡CH,乙醛与甲醛发生加成反应生成C,C与氢气发生加成反应生成D为HOCH2CH2CH2OH.由H的结构可知, 与氯气发生取代反应生成F为
与氯气发生取代反应生成F为 ,G为
,G为 ,F氧化生成
,F氧化生成 ,H与HOCH2CH2CH2OH发生缩聚反应得到PTT为
,H与HOCH2CH2CH2OH发生缩聚反应得到PTT为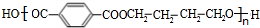 .
.
(1)A与水发生加成反应生成B(乙醛),则A的分子式为C2H2,故答案为:C2H2;
(2)D为HOCH2CH2CH2OH,系统命名法命名为:1,4-丁二醇,故答案为:1,4-丁二醇;
(3)a.CH2O为甲醛,与乙醛互为同系物,故a正确;
b.C2H4O可能为乙醛,也可能为环氧乙烷,与乙醛不是同系物,故b错误;
c.C3H4O可能为丙酮、丙醛,与乙醛不一定是同系物,故c错误;
d.2-甲基丁醛与乙醛互为同系物,故d正确,
故选:ad;
(4)由D与H合成PTT的化学方程式为:n +n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$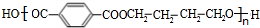 +(2n-1)H2O,属于缩聚反应,
+(2n-1)H2O,属于缩聚反应,
故答案为:n +n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$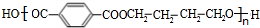 +(2n-1)H2O,缩聚反应;
+(2n-1)H2O,缩聚反应;
(5)有机物G( )的同分异构体同时符合下列条件:①能与FeCl3溶液发生显色反应,说明含有酚羟基,②苯环上只有三个取代基,③分子中含有两个-OH,
)的同分异构体同时符合下列条件:①能与FeCl3溶液发生显色反应,说明含有酚羟基,②苯环上只有三个取代基,③分子中含有两个-OH,
取代基可以是2个-OH与-CH2CH3,2个-OH处于邻位,-CH2CH3有2种位置,2个-OH处于间位,-CH2CH3有3种位置,2个-OH处于对位,-CH2CH3有1种位置;
取代基可以是-CH2OH、-OH、-CH3,而-CH2OH、-OH有邻、间、对,对应的-CH3分别有4、4、2中位置,符合条件的同分异构体共有16种,其中核震共振氢谱显示有5组峰,且峰面积之比为3:2:2:2:1的是 等,
等,
故答案为:16; .
.
点评 本题考查有机物的推断与合成,充分利用有机物的结构简式及反应条件进行分析,熟练掌握官能团的性质与转化,是对有机化学基础的综合考查,较好的考查学生分析推理能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | W、Y、Z的非金属性大小顺序一定是Z>Y>W | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | W、Z形成的某化合物常可用作萃取剂 | |
| D. | WY2分子中既有非极性键又有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
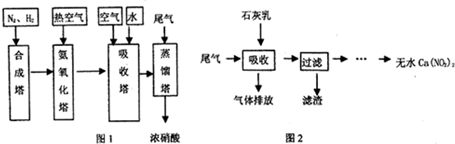
 CO+3H2. 在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过反应CO(g)+H2O(g)?CO2(g)+H2(g)来实现.己知1100K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O):c(CO)不低于5.8:1.
CO+3H2. 在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过反应CO(g)+H2O(g)?CO2(g)+H2(g)来实现.己知1100K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O):c(CO)不低于5.8:1. 6xH2O+(2x+3)N2.
6xH2O+(2x+3)N2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该粒子不显电性 | |
| B. | 该粒子的质量数与${\;}_{z}^{4}$He的相同,两者互为同位素 | |
| C. | 在元素周期表中与氢元素占同一位置 | |
| D. | 1mol该粒子的质量为8g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:d>b | |
| B. | 最高价氧化物对应水化物的酸性:d>c | |
| C. | 化合物ac2中含有离子键 | |
| D. | 氧元素分别与a、b形成的化合物都是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第ⅠA族的元素全部是金属元素 | |
| B. | 元素周期表有18个纵行,即18个族 | |
| C. | 短周期是第一、二、三、四周期 | |
| D. | 元素周期表有七个横行,也是七个周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径B>A>C>D | B. | 原子序数 a>b>c>d | ||
| C. | 离子半径C3->D->B+>A2+ | D. | 离子的还原性C3->D- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NH4+、Cl-、H+、OH-的溶液中,离子浓度是c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | pH=5的NH4Cl溶液与pH=5的硫酸中,水电离的c(H+)相同 | |
| C. | pH=9的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 将0.2 mol•L-1 CH3COOH溶液和0.1 mol•L-1NaOH溶液等体积混合,则反应后的混合溶液中:2c(OH-)+c(CH3COO-)=2c(H+)+c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com