


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
A.①中水的电离程度最小,③中水的电离程度最大
B.将②③混合,若有pH=7,则消耗溶液的体积:②>③
C.将四份溶液稀释相同倍数后,溶液的pH:③>④,②>①
D.将①④混合,若有c(CH3COO-)>c(H+),则混合液一定呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
铝可以从铝土矿中获取,铝土矿是不纯净的铝的氧化物(杂质为Fe2O3和SiO2),它是非再生资源。假如我们对铝的消费保持现有速度,我们能获得生产足够的铝所需的铝土矿仅能维持30年左右。由此看来,保护现有自然资源和对非再生资源的再利用,是值得我们考虑的。但是在废物回收过程中,仍有相当大的难度,其关键的因素主要涉及旧金属的收集与其他废物的分离、回收和提炼金属的费用、金属本身的价值等。
(1)试说明回收铝的过程中存在的困难。
(2)为什么金的回收率比铝的回收率要大得多?
(3)常温下,SiO2同强碱或强酸是很难反应的,现利用盐酸、氢氧化钠溶液、氮气、二氧化碳和水,从铝土矿中提取纯净的Al2O3。试设计一个适用于工业生产上提纯Al2O3的实验方案,用化学方程式表示提纯的过程。
(4)制取1 mol Al理论上需要多少库仑的电量(已知1 mol电子电量约为105C)?
(5)假定用6 V的直流电源进行电解,制2.7吨铝需要多少千焦的电能?(请列式并计算)
(6)在1.01×105 Pa,27 ℃时,每生产1 mol Al,理论上在阳极生成O2的体积为多少升?(请列式并计算)
(7)如果每度电的费用为0.60元,试计算生产厂家每生产1吨铝需付出的电费为多少元。(1度电=3 600 kJ)(请列式计算)
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)
运用化学反应原理研究氮、氧等元素的单质及其化合物的反应有重要意义。
Ⅰ.(1)一定温度和压强下,反应N2(g) + 3H2(g) 2NH3(g)达到化学平衡状态。若向平衡体系中通入氩气,平衡 (填“向左”、“向右”或“不”)移动;若使用活性更强的催化剂,该反应的ΔH (填“增大”、“减小”或“不改变”)。
(2)在一定温度和压强下,已知:
O2 (g) = O2+(g) + e-;![]() H1= 1175.7 kJ/mol
H1= 1175.7 kJ/mol
PtF6 (g) + e-= PtF6- (g);![]() H2= ―771.1 kJ/mol
H2= ―771.1 kJ/mol
O2PtF6 (s)= O2+ (g) + PtF6- (g);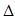 H3=482.2 kJ/mol
H3=482.2 kJ/mol
则反应O2 (g) + PtF6 (g) =O2PtF6 (s);![]() H=_____________ kJ/mol。
H=_____________ kJ/mol。
Ⅱ.现有常温下的六种溶液:①0.01 mol/L CH3COOH溶液;②0.01 mol/L HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01mol/L CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01 mol/L HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)⑤、⑥溶液比较,pH较大的是 。
(2)六种溶液中,水的电离程度相同的是______________。
(3)若②、③混合后所得溶液pH=7,则消耗溶液的体积:②________ ③(选填“>”、“<”或“=”)。
(4)稀释相同倍数后,溶液的pH:① ②,③ ④(选填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2011-2011-2012学年广东省韶关市高三下学期第二次调研考试化学试卷(解析版) 题型:填空题
(16分)草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂。草酸的盐可用作碱土金属离子的广谱沉淀剂。
(1)40 ℃时混合一定体积的0.1 mol/L H2C2O4溶液与一定体积0.01 mol/L酸性KMnO4溶液,填写表中空格。
|
温度 |
v(H2C2O4) |
v(KMnO4) |
KMnO4褪色时间 |
|
40 ℃ |
10 ml |
10 ml |
40 s |
|
40 ℃ |
20 ml |
20 ml |
|
(2)用甲基橙作指示剂,通过酸碱滴定可测定草酸溶液浓度。甲基橙是一种常用的酸碱指示剂,甲基橙(用化学式HIn表示)本身就是一种有机弱酸,其电离方程式为:HIn H++In—。则酸根离子In—的颜色是
。甲基橙的酸性与草酸相比,
(填前者强、前者弱、十分接近、无法判断)。
H++In—。则酸根离子In—的颜色是
。甲基橙的酸性与草酸相比,
(填前者强、前者弱、十分接近、无法判断)。
(3)常温下有pH均为3的盐酸和草酸溶液各10 ml,加水稀释,在答题卷上画出稀释过程中[来源:Z*xx*k.Com]两种溶液中c(H+)变化的示意图并作必要的标注。
(4)常温下MgC2O4的Ksp=8.1×10-5,已知当溶液中某离子的浓度≤10-5 mol/L时可认为该离子已沉淀完全。现为了沉淀1 L0.01 mol/LMgCl2溶液中的Mg2+,加入100 mL0.1 mol/L的(NH4)2C2O4溶液,通过计算判断Mg2+是否已沉淀完全。
(5)(NH4)2C2O4溶液因NH4+水解程度稍大于C2O42-而略显酸性,0.1 mol/L(NH4)2C2O4溶液pH值6.4。现有某未知溶液,常温下由水电离出的c(H+)=1.0×10-5 mol/L,该溶液pH可能是 (填字母)。
A.5 B.6 C.7 D.9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com