
| A�������رմ��ţ��㵽���� |
| B�������ڵأ��۲�����仯 |
| C��������ţ����ݵ�ת�� |
| D����ʪë����ס��ǻ�ͱ��ӣ����Ϸ���ߣ�Ѹ���뿪���� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 h��Ӧ������ȫ�������е�N2Ũ��Ϊ0.55 mol?L-1 |
| B��ǰ20 min��NH3��ʾ�ķ�Ӧ����Ϊ0.01 mol?L-1?min-1 |
| C������H2��Ũ�Ȼ��¶ȣ�ƽ�⽫������Ӧ�����ƶ����ҷ�Ӧ���ʾ��ӿ� |
| D����������ѹǿ���ı�ʱ��˵����Ӧ�Ѵﵽƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
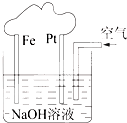
| A������һ������װ�� |
| B�����ǵ��NaOH��Һ��װ�� |
| C����װ����FeΪ�������缫��ӦΪ��Fe-2e-+2OH-=Fe��OH��2 |
| D����װ����PtΪ�������缫��ӦΪ��O2+2H2O+4e-=4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ձ���һ�����ᷢ�������ӷ�Ӧ�У�2Na+2H2O=2Na++2OH-+H2�� |
| B�������ձ����ƾ���Һ���Ͼ��ҷ�Ӧ����ȶ��ԣ�X�ձ��еķ�Ӧƽ��Щ |
| C��Z�ձ���һ�����г������ɣ����������ǵ���ͭ |
| D�������ձ����û�������������ʵ���һ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.45moL |
| B������0.45moL |
| C����0.45-0.90 moL ֮�� |
| D������0.90 moL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Al3+��Na+��NO3-��Cl- |
| B��K+��Na+��Cl-��SO42- |
| C��K+��Na+��Cl-��CO32- |
| D��K+��Cu2+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��O3��O2��Ϊͬλ�� |
| B��O3��O2�ȶ� |
| C����������O3��O2������ͬ��ԭ���� |
| D��O3��O2���ת���������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1molH2O������Ϊ18g/mol |
| B��CH4��Ħ������Ϊ16g |
| C��3.01��1023��SO2���ӵ�����Ϊ32g |
| D��2molNaOH����1Lˮ�������Һ��Ũ��Ϊ2mol?L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com