
| A、Na2HPO4 |
| B、NaHSO4 |
| C、(NH4)2SO4 |
| D、K2S |


科目:高中化学 来源: 题型:
| A、钠可以保存在煤油或四氯化碳中 |
| B、钠长久露置在空气中最终生成NaHCO3 |
| C、钠在空气中燃烧,火焰黄色,生成淡黄色的Na2O2 |
| D、钠与水反应的实验现象可以说明钠硬度小、熔点低、密度小于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HgCl2属于离子化合物 |
| B、HgCl2属于共价化合物 |
| C、HgCl2属于非电解质 |
| D、HgCl2是弱酸弱碱盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液氨可用作致冷剂 |
| B、向Fe( OH ) 3 胶体中滴入过量的NaHSO4溶液,能使胶体发生凝聚而沉淀 |
| C、熔融状态下能够导电的化合物中一定存在离子键 |
| D、28g 乙烯和氮气的混合气体中含有NA个原子(戈代表阿伏加德罗常数的值) |
查看答案和解析>>
科目:高中化学 来源: 题型:
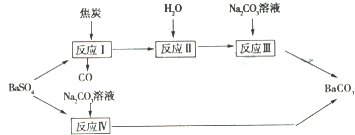
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com