
ijl00mL��Һ���ܺ���Na+��NH4+��Fe3+��CO32 -��SO42 -��Cl-�е������֣�ȡ����Һ��������ʵ�飬ʵ�������ͼ���������Լ�������������ȫ���ݳ�������˵������ȷ����( )
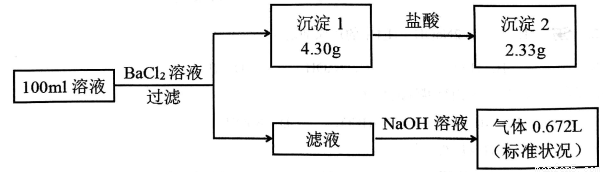
A. ԭ��Һһ������CO32 -��SO42 -��һ��������Fe3+
B. �Ƿ����Na+ֻ��ͨ����ɫ��Ӧ����ȷ��
C. ԭ��Һһ������Na+�����ܴ���Cl-
D. ��ԭ��Һ�в�����Cl-����c (Na+) =0.1mol��L-1
 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ʡɳ��2016-2017ѧ��߶���ѧ�ڵ�����˫�ܿ���ѧ�Ծ���A���� ���ͣ������
X��Y��M��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2�Ǻ���ɫ���壻X����Ԫ�ؿ��γ�XH3��M�����ڱ��е縺������Ԫ�أ�Z��̬ԭ�ӵ�M����K���������3����R2�����ӵ�3d�������9�����ӡ���ش��������⣺
��1����̬Yԭ�ӵļ۵����Ų�ͼ��______��Z���������е�һ��������������Ԫ����_______��Ԫ�����ƣ�
��2��XY2? ���ӵ����幹����________��R2����ˮ������[R��H2O��4]2+�У��ṩ�µ��ӶԵ�ԭ����________��Ԫ�ط��ţ���
��3����֪XH3����R2+�γ������ӣ���XM3������R2+�γ������ӣ���ԭ����_______________��
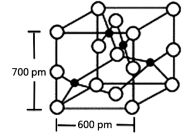
��4��Y��R���γɵĻ����ᄃ�徧����ͼ��ʾ,�þ���Ļ�ѧʽ:_____________������������ͼ��ʾ����þ����ܶ���___________g?cm-3����ʽ��������������С�������һλ����
��5��ͼ1��ʾij�ֺ����л�������Ľṹ���������4����ԭ�ӷֱ�λ�����������4�����㣨��ͼ2���������ڴ��ڿ�ǻ����Ƕ��ij���ӻ���Ӳ��γ�4���������ʶ�����з��ӻ������У��ܱ����л�������ʶ�����________�����ţ���
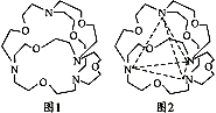
a��CF4 b��CH4 c��NH4+ d��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��������߶���ѧ����ĩ��⻯ѧ�Ծ��������棩 ���ͣ�ʵ����
����ij��ѧ��ȤС��Ҫ����к��ȵIJⶨ���ش��������⣺
��1��ʵ�����ϱ��д�С�����ձ�����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β����������0.5mol•L��1���ᡢ0.55mol•L��1NaOH��Һ��ʵ����ȱ�ٵIJ�����Ʒ��_______��
��2����֪����Ӧ����Һ�ı�����cΪ4.18J���橁1•g��1��0.5mol•L��1�����0.55mol��L��1NaOH��Һ���ܶȾ�Ϊ1g��cm��3��ʵ��ʱ��¼��ʵ���������£�
ʵ�� ���� | ��Ӧ�P���� | �� Һ �� �� | ||
t1 | t2 | |||
1 | 50mL0.55mol•L-1NaOH��Һ | 50mL.0.5mol•L-1HCl��Һ | 20�� | 23.3�� |
2 | 50mL0.55mol•L-1NaOH��Һ | 50mL.0.5mol•L-1HCl��Һ | 20�� | 23.5�� |
��������������Ʒ�Ӧ���к��ȡ�H1=____________��������λС����
����֪��CH3COOH(aq) CH3COO-(aq)+H+(aq) ��H2>0 ,
CH3COO-(aq)+H+(aq) ��H2>0 ,
CH3COOH(aq)+OH-(aq)= CH3COO-(aq)+H20(l) ��H3 ���H3_____��H1���>������<������=����
����ijʵ��С�����������ữ��KMnO4��H2C2O4��Ӧ��̽������������Ի�ѧ��Ӧ���ʵ�Ӱ�족����С��ʵ�鷽������(ʵ��ⶨKMnO4��Һ��ȫ��ɫʱ��)���ش��������⣺
ʵ�� ��� | H2C2O4��Һ | ����KMnO4��Һ | H2O/mL | �¶�/�� | KMnO4��Һ��ȫ��ɫʱ�䣨s�� | ||
Ũ��/mol��L-1 | ���/mL | Ũ��/mol��L-1 | ���/mL | ||||
�� | 0.20 | 2.0 | 0.010 | 4.0 | 2.0 | 25 | t1 |
�� | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 25 | t2 |
�� | 0.20 | 4.0 | 0.010 | 4.0 | 0 | 50 | t3 |
��3��������Ӧ�����ӷ���ʽΪ______________________________________
��4��t1_____ t2���>������<������=��������������__________________
��5��ʵ��ں�ʵ�������ʵ���Ŀ����______________________________
��6����ͬѧ��ʵ��ʱ���֣������ữ��KMnO4��H2C2O4��Ӧ��ʼʱ����Һ��ɫ��������Ӧһ��ʱ�����Һ��ɫ���Լӿ졣�������ʵ������ͬѧ������в��룺
����٣������ữ��KMnO4��H2C2O4��Ӧ�Ƿ��ȷ�Ӧ��������Һ�¶����ߣ���Ӧ���ʼӿ졣
����ڣ�__________________�����㲹�䣩
Ҫ֤ʵ����ڣ��������ữ�ĸ��������Һ��������Һ�⣬����Ҫѡ����Լ���______��
A.����� B.������ C.ˮ D.�Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��������߶���ѧ����ĩ��⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ��������������ȷ����
A. ��16g��ԭ�ӵĶ������辧���к��еĦҼ���ĿΪ2NA
B. 1mol��(��CH3)����������Ϊ9NA
C. 12��ʯī�к��еĹ��ۼ���ĿΪ1.5NA
D. 2molSO2��1molO2��һ�������·�Ӧ���û���������������2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ������ɫ�������˸���3����Ӧ�Կ��ԣ�ѡ������ѧ�Ծ��������棩 ���ͣ������
Һ��������ֽ��������������Ϊȼ�Ϲ�������ȼ�ϵ�ء�
��֪��2NH3(g)  N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1
N2 (g)+3H2(g) ��H= 92.4 kJ��mol-1
2H2 (g)+O2 (g)=2H2O(g) ��H= - 483.6 kJ��mol-1
NH3(l)  NH3 (g) ��H= 23.4 kJ��mol-1
NH3 (g) ��H= 23.4 kJ��mol-1
(1) 4NH3(l)+3O2 (g) 2N2(g)+6H2O(g) �ġ�H=______���÷�Ӧ��ƽ�ⳣ������ʽΪ______��
2N2(g)+6H2O(g) �ġ�H=______���÷�Ӧ��ƽ�ⳣ������ʽΪ______��
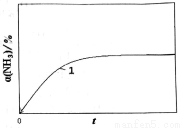
(2) 2NH3(g)  N2(g)ʮ3H2(g)���Է���������_________������¡����¡��������£�T1������ʱ�����ֽ��ʼŨ��Ϊc0�İ������ð�����ת���ʦ�(NH3)��ʱ��t�仯�Ĺ�ϵ��ͼ����1��������������������䣬����Ӧ�¶���ߵ�T2������ͼ��������һ�����ֽ��ʼŨ��ҲΪc0�İ��������Ц�(NH3)��t������������_________����ע2����
N2(g)ʮ3H2(g)���Է���������_________������¡����¡��������£�T1������ʱ�����ֽ��ʼŨ��Ϊc0�İ������ð�����ת���ʦ�(NH3)��ʱ��t�仯�Ĺ�ϵ��ͼ����1��������������������䣬����Ӧ�¶���ߵ�T2������ͼ��������һ�����ֽ��ʼŨ��ҲΪc0�İ��������Ц�(NH3)��t������������_________����ע2����
(3)���о����������¶ȴ���70�桢������������Һ�У���ͨ����ⷨ��ԭ�����õ�������д�������ĵ缫��Ӧʽ______________________��
(4) 25��ʱ����amol/L�İ�ˮ��b mol/L����������ϣ�����仯���Բ��ƣ�����Ӧ����Һǡ�������ԣ���a��b��ʾNH3��H2O�ĵ���ƽ�ⳣ��Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ������ɫ�������˸���3����Ӧ�Կ��ԣ�ѡ������ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ�ֱ����NaCl�����ʯ���ɱ���ʯī�ṹ��һ���֡�����˵����ȷ����( )
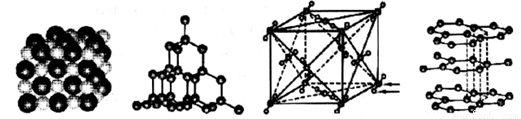
A. NaCl����ֻ��������״̬�����Ӽ�����ȫ�ƻ��������γ������ƶ�������
B. ���ʯ�д��ڵĻ�ѧ��ֻ�й��ۼ������ܵ���
C. �ɱ��еĻ�ѧ��ֻ�����պ��ٵ������Ϳ����ƻ������Ըɱ���������
D. ʯī��̼ԭ�ӵ��������Ӷ������˹��ۼ����γɣ����۵�ܸߡ�Ӳ�Ⱥܴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ������ɫ�������˸���3����Ӧ�Կ��ԣ�ѡ������ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����( )
A. NaHCO3��Һ������ij���ʯ��ˮ��Ӧ��Ca2++OH-+HCO3-=CaCO3��+H2O
B. ��ʳ�׳�ȥ��ˮƿˮ����CaCO3��CaCO3+2H+=Ca2++CO2��+H2O
C. ������������Һ�еμ�����ϡ���Ba2++OH-+SO42 -+H+=BaSO4��+H2O
D. �����ƺ�ˮ��Ӧ��Na+2H2O=Na++2OH-+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ2016-2017ѧ���һ3���¿���ѧ�Ծ� ���ͣ������
����·�Ӧ�Ļ�ѧ��ףʽ�����ӷ���ʽ:
��1�������ɫ���Ļ�����д��ԣ���Ӧ_____________��
��2����ҵ���ƴֹ�ķ�Ӧ____________��
��3����������Һ�м��������ˮ�����ӷ���ʽ____________��
��4����ϡ������ϴͭ��������ϵ�ͭ������ӷ���ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶���ѧ�ڵ�һ���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
��11�֣����û�ѧ��Ӧԭ���о�������ȵ��ʼ��仯����ķ�Ӧ����Ҫ���塣
��1����������������2SO2(g)��O2(g�� 2SO3(g)��ƽ������ϵ��SO3 �İٷֺ������¶ȵĹ�ϵ��ͼ��ʾ������ͼ�ش��������⣺
2SO3(g)��ƽ������ϵ��SO3 �İٷֺ������¶ȵĹ�ϵ��ͼ��ʾ������ͼ�ش��������⣺
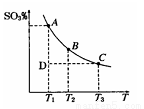
��2SO2(g)+O2(g�� 2SO3(g)�ġ�H________0���>����<������
2SO3(g)�ġ�H________0���>����<������
��һ�������£���SO2��O2�������2:1����һ���������ܱ������з������Ϸ�Ӧ����˵���÷�Ӧ�Ѵﵽƽ�����________��
a����ϵ���ܶȲ������仯
b��SO2��SO3������ȱ��ֲ���
c����ϵ����Ԫ�ص������ٷֺ������ٱ仯
d����λʱ����ת��4 mol ���ӣ�ͬʱ����2 mol SO3
e�������ڵ���������������ٱ仯
��2��һ���������£��ϳɰ���ӦΪ��N2(g)+3H2(g�� 2NH3(g)��ͼ1��ʾ�ڴ˷�Ӧ�����е������ı仯��ͼ2��ʾ��2L���ܱ������з�ӦʱN2�����ʵ�����ʱ��ı仯���ߡ�ͼ3��ʾ�������������������£��ı���ʼ�����������ʵ����Դ˷�Ӧƽ���Ӱ�졣
2NH3(g)��ͼ1��ʾ�ڴ˷�Ӧ�����е������ı仯��ͼ2��ʾ��2L���ܱ������з�ӦʱN2�����ʵ�����ʱ��ı仯���ߡ�ͼ3��ʾ�������������������£��ı���ʼ�����������ʵ����Դ˷�Ӧƽ���Ӱ�졣
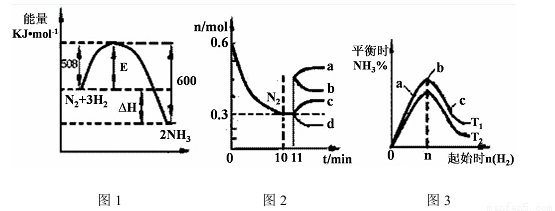
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ �������¶ȣ�ƽ�ⳣ�� �������С�����䡱����
����ͼ2��Ϣ������0~10min�ڸ÷�Ӧ��ƽ������v(H2)= ����11min�������������䣬ѹ�����������Ϊ1L����n(N2)�ı仯����Ϊ (�a����b����c����d��)
��ͼ3 a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ��� �㣬�¶�T1 T2���>����=����<����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com