
| A. | K+、AlO2-、Cl-、SO42- | B. | Fe2+、HCO3-、K2、SO42- | ||
| C. | Na+、Cl-、AlO2-、NO3- | D. | NH4+、NO3-、I-、CO32- |
分析 加入足量Na2O2后,与水反应生成NaOH和氧气,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:加入足量Na2O2后,与水反应生成NaOH和氧气,
A.该组离子之间不反应,可大量共存,故A正确;
B.碱性溶液中不能大量存在HCO3-,且Fe2+、Na2O2发生氧化还原反应,不能共存,故B错误;
C.该组离子之间不反应,可大量共存,故C正确;
D.碱性溶液中不能大量存在NH4+,且I-、Na2O2发生氧化还原反应,不能共存,故D错误;
故选AC.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的判断,题目难度不大.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题
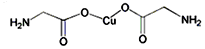
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池是常见的二次电池,性能优良,比能量高,缺点是废弃电池铅污染严重 | |
| B. | 用玻璃棒蘸取KMnO4(H+)溶液,滴在pH试纸上,然后与标准比色卡对照,测定其pH | |
| C. | 石油的分馏、蛋白质的盐析、焰色反应、煤的液化与气化都是物理变化 | |
| D. | 在元素周期表的金属和非金属分界线附近可寻找锗、硅、硒等半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F、Cl、Br、I最高正化合价都为+7 | |
| B. | 卤族元素的单质只有氧化性 | |
| C. | 从F到I,原子的得电子能力依次加强 | |
| D. | 卤素单质与H2化合的难易程度按F2、Cl2、Br2、I2的顺序由易变难 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ④⑥ | C. | ③⑥ | D. | ③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水淡化的方法有蒸馏法、离子交换法、电渗析法等 | |
| B. | 明矾水解时能生成具有吸附性的胶体粒子,故可用于消毒杀菌 | |
| C. | Ba2+对人体无毒,故BaSO4在医学上可用作“钡餐” | |
| D. | 与铜质水龙头连接处的铜质水管不易发生腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com